- Калорийность Печень говяжья. Химический состав и пищевая ценность.
- Говяжья печень — аминокислотный состав
- Говяжья печень — калорийность (сколько калорий в 100 граммах)
- Говяжья печень — сколько углеводов (на 100 грамм)
- Говяжья печень – калорийность, полезные свойства, польза и вред, описание
- Печень говяжья – описание, состав, калорийность и пищевая ценность
- польза и вред, состав и противопоказания.
- Печень: анатомия и функции | Johns Hopkins Medicine
- Печень | Безграничная анатомия и физиология
- Печень | анатомия | Britannica
- Структурные и функциональные аспекты печени и синусоидальных клеток печени в связи с метастазами карциномы толстой кишки
- Структурные и функциональные аспекты печени и синусоидальных клеток печени в связи с метастазами карциномы толстой кишки
- Структурные и функциональные аспекты печени и синусоидальных клеток печени в связи с метастазами карциномы толстой кишки
- Структурные и функциональные аспекты печени и синусоидальных клеток печени в связи с метастазами карциномы толстой кишки
Калорийность Печень говяжья. Химический состав и пищевая ценность.
Печень говяжья богат такими витаминами и минералами, как: витамином А – 929,7 %, бэта-каротином – 20 %, витамином B1 – 20 %, витамином B2 – 121,7 %, холином – 127 %, витамином B5 – 136 %, витамином B6 – 35 %, витамином B9 – 60 %, витамином B12 – 2000 %, витамином C – 36,7 %, витамином D – 12 %, витамином H – 196 %, витамином PP – 65 %, калием – 11,1 %, фосфором – 39,3 %, железом – 38,3 %, кобальтом – 199 %, марганцем – 15,8 %, медью – 380 %, молибденом – 157,1 %, селеном – 72,2 %, хромом – 64 %, цинком – 41,7 %- Витамин А отвечает за нормальное развитие, репродуктивную функцию, здоровье кожи и глаз, поддержание иммунитета.
- В-каротин является провитамином А и обладает антиоксидантными свойствами. 6 мкг бета-каротина эквивалентны 1 мкг витамина А.
- Витамин В1 входит в состав важнейших ферментов углеводного и энергетического обмена, обеспечивающих организм энергией и пластическими веществами, а также метаболизма разветвленных аминокислот.

- Витамин В2 участвует в окислительно-восстановительных реакциях, способствует повышению восприимчивости цвета зрительным анализатором и темновой адаптации. Недостаточное потребление витамина В2 сопровождается нарушением состояния кожных покровов, слизистых оболочек, нарушением светового и сумеречного зрения.
- Холин входит в состав лецитина, играет роль в синтезе и обмене фосфолипидов в печени, является источником свободных метильных групп, действует как липотропный фактор.
- Витамин В5 участвует в белковом, жировом, углеводном обмене, обмене холестерина, синтезе ряда гормонов, гемоглобина, способствует всасыванию аминокислот и сахаров в кишечнике, поддерживает функцию коры надпочечников. Недостаток пантотеновой кислоты может вести к поражению кожи и слизистых.
- Витамин В6 участвует в поддержании иммунного ответа, процессах торможения и возбуждения в центральной нервной системе, в превращениях аминокислот, метаболизме триптофана, липидов и нуклеиновых кислот, способствует нормальному формированию эритроцитов, поддержанию нормального уровня гомоцистеина в крови.
 Недостаточное потребление витамина В6 сопровождается снижением аппетита, нарушением состояния кожных покровов, развитием гомоцистеинемии, анемии.
Недостаточное потребление витамина В6 сопровождается снижением аппетита, нарушением состояния кожных покровов, развитием гомоцистеинемии, анемии. - Витамин В9 в качестве кофермента участвуют в метаболизме нуклеиновых и аминокислот. Дефицит фолатов ведет к нарушению синтеза нуклеиновых кислот и белка, следствием чего является торможение роста и деления клеток, особенно в быстро пролифелирующих тканях: костный мозг, эпителий кишечника и др. Недостаточное потребление фолата во время беременности является одной из причин недоношенности, гипотрофии, врожденных уродств и нарушений развития ребенка. Показана выраженная связь между уровнем фолата, гомоцистеина и риском возникновения сердечно-сосудистых заболеваний.
- Витамин В12 играет важную роль в метаболизме и превращениях аминокислот. Фолат и витамин В12 являются взаимосвязанными витаминами, участвуют в кроветворении. Недостаток витамина В12 приводит к развитию частичной или вторичной недостаточности фолатов, а также анемии, лейкопении, тромбоцитопении.

- Витамин С участвует в окислительно-восстановительных реакциях, функционировании иммунной системы, способствует усвоению железа. Дефицит приводит к рыхлости и кровоточивости десен, носовым кровотечениям вследствие повышенной проницаемости и ломкости кровеносных капилляров.
- Витамин D поддерживает гомеостаз кальция и фосфора, осуществляет процессы минерализации костной ткани. Недостаток витамина D приводит к нарушению обмена кальция и фосфора в костях, усилению деминерализации костной ткани, что приводит к увеличению риска развития остеопороза.
- Витамин Н участвует в синтезе жиров, гликогена, метаболизме аминокислот. Недостаточное потребление этого витамина может вести к нарушению нормального состояния кожных покровов.
- Витамин РР участвует в окислительно-восстановительных реакциях энергетического метаболизма. Недостаточное потребление витамина сопровождается нарушением нормального состояния кожных покровов, желудочно- кишечного тракта и нервной системы.

- Калий является основным внутриклеточным ионом, принимающим участие в регуляции водного, кислотного и электролитного баланса, участвует в процессах проведения нервных импульсов, регуляции давления.
- Фосфор принимает участие во многих физиологических процессах, включая энергетический обмен, регулирует кислотно-щелочного баланса, входит в состав фосфолипидов, нуклеотидов и нуклеиновых кислот, необходим для минерализации костей и зубов. Дефицит приводит к анорексии, анемии, рахиту.
- Железо входит в состав различных по своей функции белков, в том числе ферментов. Участвует в транспорте электронов, кислорода, обеспечивает протекание окислительно- восстановительных реакций и активацию перекисного окисления. Недостаточное потребление ведет к гипохромной анемии, миоглобиндефицитной атонии скелетных мышц, повышенной утомляемости, миокардиопатии, атрофическому гастриту.
- Кобальт входит в состав витамина В12. Активирует ферменты обмена жирных кислот и метаболизма фолиевой кислоты.

- Марганец участвует в образовании костной и соединительной ткани, входит в состав ферментов, включающихся в метаболизм аминокислот, углеводов, катехоламинов; необходим для синтеза холестерина и нуклеотидов. Недостаточное потребление сопровождается замедлением роста, нарушениями в репродуктивной системе, повышенной хрупкостью костной ткани, нарушениями углеводного и липидного обмена.
- Медь входит в состав ферментов, обладающих окислительно-восстановительной активностью и участвующих в метаболизме железа, стимулирует усвоение белков и углеводов. Участвует в процессах обеспечения тканей организма человека кислородом. Дефицит проявляется нарушениями формирования сердечно-сосудистой системы и скелета, развитием дисплазии соединительной ткани.
- Молибден является кофактором многих ферментов, обеспечивающих метаболизм серусодержащих аминокислот, пуринов и пиримидинов.
- Селен – эссенциальный элемент антиоксидантной системы защиты организма человека, обладает иммуномодулирующим действием, участвует в регуляции действия тиреоидных гормонов.

- Хром участвует в регуляции уровня глюкозы крови, усиливая действие инсулина. Дефицит приводит к снижению толерантности к глюкозе.
- Цинк входит в состав более 300 ферментов, участвует в процессах синтеза и распада углеводов, белков, жиров, нуклеиновых кислот и в регуляции экспрессии ряда генов. Недостаточное потребление приводит к анемии, вторичному иммунодефициту, циррозу печени, половой дисфункции, наличию пороков развития плода. Исследованиями последних лет выявлена способность высоких доз цинка нарушать усвоение меди и тем способствовать развитию анемии.
Полный справочник самых полезных продуктов вы можете посмотреть в приложении «Мой здоровый рацион».
Говяжья печень — аминокислотный состав
Категория продуктов
Все продукты
Мясо
Мясо убойных животных
Мясо диких животных (дичь)
Субпродукты
Мясо птицы (и субпродукты)
Рыба
Морепродукты (все категории)
Моллюски
Ракообразные (раки, крабы, креветки)
Морские водоросли
Яйца, яичные продукты
Молоко и молочные продукты (все категории)
Сыры
Молоко и кисломолочные продукты
Творог
Другие продукты из молока
Соя и соевые продукты
Овощи и овощные продукты
Клубнеплоды
Корнеплоды
Капустные (овощи)
Салатные (овощи)
Пряные (овощи)
Луковичные (овощи)
Паслёновые
Бахчевые
Бобовые
Зерновые (овощи)
Десертные (овощи)
Зелень, травы, листья, салаты
Фрукты, ягоды, сухофрукты
Грибы
Жиры, масла
Сало, животный жир
Растительные масла
Орехи
Крупы, злаки
Семена
Специи, пряности
Мука, продукты из муки
Мука и отруби, крахмал
Хлеб, лепёшки и др.
Содержание нутриента
ВодаБелкиЖирыУглеводыСахараГлюкозаФруктозаГалактозаСахарозаМальтозаЛактозаКрахмалКлетчаткаЗолаКалорииКальцийЖелезоМагнийФосфорКалийНатрийЦинкМедьМарганецСеленФторВитамин AБета-каротинАльфа-каротинВитамин DВитамин D2Витамин D3Витамин EВитамин KВитамин CВитамин B1Витамин B2Витамин B3Витамин B4Витамин B5Витамин B6Витамин B9Витамин B12ТриптофанТреонинИзолейцинЛейцинЛизинМетионинЦистинФенилаланинТирозинВалинАргининГистидинАланинАспарагиноваяГлутаминоваяГлицинПролинСеринСуммарно все насыщенные жирные кислотыМасляная к-та (бутановая к-та) (4:0)Капроновая кислота (6:0)Каприловая кислота (8:0)Каприновая кислота (10:0)Лауриновая кислота (12:0)Миристиновая кислота (14:0)Пальмитиновая кислота (16:0)Стеариновая кислота (18:0)Арахиновая кислота (20:0)Бегеновая кислота (22:0)Лигноцериновая кислота (24:0)Суммарно все мононенасыщенные жирные кислотыПальмитолеиновая к-та (16:1)Олеиновая кислота (18:1)Гадолиновая кислота (20:1)Эруковая кислота (22:1)Нервоновая кислота (24:1)Суммарно все полиненасыщенные жирные кислотыЛинолевая кислота (18:2)Линоленовая кислота (18:3)Альфа-линоленовая к-та (18:3) (Омега-3)Гамма-линоленовая к-та (18:3) (Омега-6)Эйкозадиеновая кислота (20:2) (Омега-6)Арахидоновая к-та (20:4) (Омега-6)Тимнодоновая к-та (20:5) (Омега-3)Докозапентаеновая к-та (22:5) (Омега-3)Холестерин (холестерол)Фитостерины (фитостеролы)СтигмастеролКампестеролБета-ситостерин (бета-ситостерол)Всего трансжировТрансжиры (моноеновые)Трансжиры (полиеновые)BCAAКреатинАлкогольКофеинТеобромин
Говяжья печень — калорийность (сколько калорий в 100 граммах)
Категория продуктов
Все продукты
Мясо
Мясо убойных животных
Мясо диких животных (дичь)
Субпродукты
Мясо птицы (и субпродукты)
Рыба
Морепродукты (все категории)
Моллюски
Ракообразные (раки, крабы, креветки)
Морские водоросли
Яйца, яичные продукты
Молоко и молочные продукты (все категории)
Сыры
Молоко и кисломолочные продукты
Творог
Другие продукты из молока
Соя и соевые продукты
Овощи и овощные продукты
Клубнеплоды
Корнеплоды
Капустные (овощи)
Салатные (овощи)
Пряные (овощи)
Луковичные (овощи)
Паслёновые
Бахчевые
Бобовые
Зерновые (овощи)
Десертные (овощи)
Зелень, травы, листья, салаты
Фрукты, ягоды, сухофрукты
Грибы
Жиры, масла
Сало, животный жир
Растительные масла
Орехи
Крупы, злаки
Семена
Специи, пряности
Мука, продукты из муки
Мука и отруби, крахмал
Хлеб, лепёшки и др. Макароны, лапша (паста)
Сладости, кондитерские изделия
Фастфуд
Напитки, соки (все категории)
Фруктовые соки и нектары
Алкогольные напитки
Напитки (безалкогольные напитки)
Пророщенные семена
Вегетарианские продукты
Веганские продукты (без яиц и молока)
Продукты для сыроедения
Фрукты и овощи
Продукты растительного происхождения
Продукты животного происхождения
Высокобелковые продукты
Макароны, лапша (паста)
Сладости, кондитерские изделия
Фастфуд
Напитки, соки (все категории)
Фруктовые соки и нектары
Алкогольные напитки
Напитки (безалкогольные напитки)
Пророщенные семена
Вегетарианские продукты
Веганские продукты (без яиц и молока)
Продукты для сыроедения
Фрукты и овощи
Продукты растительного происхождения
Продукты животного происхождения
Высокобелковые продукты
Содержание нутриента
ВодаБелкиЖирыУглеводыСахараГлюкозаФруктозаГалактозаСахарозаМальтозаЛактозаКрахмалКлетчаткаЗолаКалорииКальцийЖелезоМагнийФосфорКалийНатрийЦинкМедьМарганецСеленФторВитамин AБета-каротинАльфа-каротинВитамин DВитамин D2Витамин D3Витамин EВитамин KВитамин CВитамин B1Витамин B2Витамин B3Витамин B4Витамин B5Витамин B6Витамин B9Витамин B12ТриптофанТреонинИзолейцинЛейцинЛизинМетионинЦистинФенилаланинТирозинВалинАргининГистидинАланинАспарагиноваяГлутаминоваяГлицинПролинСеринСуммарно все насыщенные жирные кислотыМасляная к-та (бутановая к-та) (4:0)Капроновая кислота (6:0)Каприловая кислота (8:0)Каприновая кислота (10:0)Лауриновая кислота (12:0)Миристиновая кислота (14:0)Пальмитиновая кислота (16:0)Стеариновая кислота (18:0)Арахиновая кислота (20:0)Бегеновая кислота (22:0)Лигноцериновая кислота (24:0)Суммарно все мононенасыщенные жирные кислотыПальмитолеиновая к-та (16:1)Олеиновая кислота (18:1)Гадолиновая кислота (20:1)Эруковая кислота (22:1)Нервоновая кислота (24:1)Суммарно все полиненасыщенные жирные кислотыЛинолевая кислота (18:2)Линоленовая кислота (18:3)Альфа-линоленовая к-та (18:3) (Омега-3)Гамма-линоленовая к-та (18:3) (Омега-6)Эйкозадиеновая кислота (20:2) (Омега-6)Арахидоновая к-та (20:4) (Омега-6)Тимнодоновая к-та (20:5) (Омега-3)Докозапентаеновая к-та (22:5) (Омега-3)Холестерин (холестерол)Фитостерины (фитостеролы)СтигмастеролКампестеролБета-ситостерин (бета-ситостерол)Всего трансжировТрансжиры (моноеновые)Трансжиры (полиеновые)BCAAКреатинАлкогольКофеинТеобромин
Говяжья печень — сколько углеводов (на 100 грамм)
Категория продуктов
Все продукты
Мясо
Мясо убойных животных
Мясо диких животных (дичь)
Субпродукты
Мясо птицы (и субпродукты)
Рыба
Морепродукты (все категории)
Моллюски
Ракообразные (раки, крабы, креветки)
Морские водоросли
Яйца, яичные продукты
Молоко и молочные продукты (все категории)
Сыры
Молоко и кисломолочные продукты
Творог
Другие продукты из молока
Соя и соевые продукты
Овощи и овощные продукты
Клубнеплоды
Корнеплоды
Капустные (овощи)
Салатные (овощи)
Пряные (овощи)
Луковичные (овощи)
Паслёновые
Бахчевые
Бобовые
Зерновые (овощи)
Десертные (овощи)
Зелень, травы, листья, салаты
Фрукты, ягоды, сухофрукты
Грибы
Жиры, масла
Сало, животный жир
Растительные масла
Орехи
Крупы, злаки
Семена
Специи, пряности
Мука, продукты из муки
Мука и отруби, крахмал
Хлеб, лепёшки и др. Макароны, лапша (паста)
Сладости, кондитерские изделия
Фастфуд
Напитки, соки (все категории)
Фруктовые соки и нектары
Алкогольные напитки
Напитки (безалкогольные напитки)
Пророщенные семена
Вегетарианские продукты
Веганские продукты (без яиц и молока)
Продукты для сыроедения
Фрукты и овощи
Продукты растительного происхождения
Продукты животного происхождения
Высокобелковые продукты
Макароны, лапша (паста)
Сладости, кондитерские изделия
Фастфуд
Напитки, соки (все категории)
Фруктовые соки и нектары
Алкогольные напитки
Напитки (безалкогольные напитки)
Пророщенные семена
Вегетарианские продукты
Веганские продукты (без яиц и молока)
Продукты для сыроедения
Фрукты и овощи
Продукты растительного происхождения
Продукты животного происхождения
Высокобелковые продукты
Содержание нутриента
ВодаБелкиЖирыУглеводыСахараГлюкозаФруктозаГалактозаСахарозаМальтозаЛактозаКрахмалКлетчаткаЗолаКалорииКальцийЖелезоМагнийФосфорКалийНатрийЦинкМедьМарганецСеленФторВитамин AБета-каротинАльфа-каротинВитамин DВитамин D2Витамин D3Витамин EВитамин KВитамин CВитамин B1Витамин B2Витамин B3Витамин B4Витамин B5Витамин B6Витамин B9Витамин B12ТриптофанТреонинИзолейцинЛейцинЛизинМетионинЦистинФенилаланинТирозинВалинАргининГистидинАланинАспарагиноваяГлутаминоваяГлицинПролинСеринСуммарно все насыщенные жирные кислотыМасляная к-та (бутановая к-та) (4:0)Капроновая кислота (6:0)Каприловая кислота (8:0)Каприновая кислота (10:0)Лауриновая кислота (12:0)Миристиновая кислота (14:0)Пальмитиновая кислота (16:0)Стеариновая кислота (18:0)Арахиновая кислота (20:0)Бегеновая кислота (22:0)Лигноцериновая кислота (24:0)Суммарно все мононенасыщенные жирные кислотыПальмитолеиновая к-та (16:1)Олеиновая кислота (18:1)Гадолиновая кислота (20:1)Эруковая кислота (22:1)Нервоновая кислота (24:1)Суммарно все полиненасыщенные жирные кислотыЛинолевая кислота (18:2)Линоленовая кислота (18:3)Альфа-линоленовая к-та (18:3) (Омега-3)Гамма-линоленовая к-та (18:3) (Омега-6)Эйкозадиеновая кислота (20:2) (Омега-6)Арахидоновая к-та (20:4) (Омега-6)Тимнодоновая к-та (20:5) (Омега-3)Докозапентаеновая к-та (22:5) (Омега-3)Холестерин (холестерол)Фитостерины (фитостеролы)СтигмастеролКампестеролБета-ситостерин (бета-ситостерол)Всего трансжировТрансжиры (моноеновые)Трансжиры (полиеновые)BCAAКреатинАлкогольКофеинТеобромин
Говяжья печень – калорийность, полезные свойства, польза и вред, описание
Калории, ккал:
125Углеводы, г:
4. 0
0Говяжья печень является самым востребованным из мясных субпродуктов. Вес говяжьей печени может превышать килограмм, печень представляет собой плотную пористую субстанцию буро-красного цвета, насыщенную большим количеством крови. Перед продажей говяжью печень освобождают от желчи и желчных протоков, оставляя лишь тонкую плёнку.
Печень – составная часть ливера (или потрохов), продукт употребляли в пищу с незапамятных времён. Авиценна настоятельно рекомендовал использовать говяжью печень как средство, благотворно влияющее на остроту зрения.
Печень поступает в продажу обработанной – без желчных протоков и желчного пузыря и освобожденной от крупных кровеносных сосудов. Мороженая печень поступает в виде блоков.
Калорийность говяжьей печени
Калорийность говяжьей печени составляет 125 ккал на 100 грамм продукта.
Состав и полезные свойства говяжьей печени
Продукт содержит много высококачественного животного белка, необходимого организму человека для строительства и роста клеток. В печени присутствуют практически все незаменимые аминокислоты, минеральные вещества, в частности железо, нужное для улучшения качества крови и профилактики анемии. Печень традиционно считается продуктом, повышающим уровень гемоглобина. Нужно помнить, что это относится к блюдам, приготовленным из свежей (незамороженной) печени. Витамин А сохраняет зрительные функции на длительный срок, предотвращает возникновение «куриной слепоты», витамин В12 принимает участие в создании и укреплении миелиновых оболочек красных кровяных телец и нервных клеток (calorizator). В говяжьей печени меньше холестерина, чем в куриной или свиной, это следует знать тем, у кого повышен уровень холестерина в крови.
В печени присутствуют практически все незаменимые аминокислоты, минеральные вещества, в частности железо, нужное для улучшения качества крови и профилактики анемии. Печень традиционно считается продуктом, повышающим уровень гемоглобина. Нужно помнить, что это относится к блюдам, приготовленным из свежей (незамороженной) печени. Витамин А сохраняет зрительные функции на длительный срок, предотвращает возникновение «куриной слепоты», витамин В12 принимает участие в создании и укреплении миелиновых оболочек красных кровяных телец и нервных клеток (calorizator). В говяжьей печени меньше холестерина, чем в куриной или свиной, это следует знать тем, у кого повышен уровень холестерина в крови.
Вред говяжьей печени
Говяжья печень практически не имеет противопоказаний, продукт является слабым аллергеном, поэтому печень вводят в прикорм малышей с года. Чрезмерное употребление печени может спровоцировать обострение панкреатита и заболеваний желчного пузыря.
Выбор и хранение говяжьей печени
Приобретая говяжью печень следует обратить внимание на внешний вид продукта, поверхность печени должна быть гладкая, красно-коричневого цвета с глянцевым блеском. При нажатии на свежую печень, она должна быстро восстановить первоначальную форму, быть упругой. Наличие большого количества жира и крупных кровеносных сосудов должно стать поводом поискать другой продукт. Запах свежей говяжьей печени чуть сладковатый, специфический. Свежую говяжью печень хранят в холодильнике не дольше суток, не закрывая плотно.
При нажатии на свежую печень, она должна быстро восстановить первоначальную форму, быть упругой. Наличие большого количества жира и крупных кровеносных сосудов должно стать поводом поискать другой продукт. Запах свежей говяжьей печени чуть сладковатый, специфический. Свежую говяжью печень хранят в холодильнике не дольше суток, не закрывая плотно.
Свежую печень можно заморозить и хранить в морозильной камере от трёх до шести месяцев. Покупая замороженную печень, нужно выбирать куски яркого цвета, без видимых тёмных и светло-коричневых пятен, без обледенения и повреждений упаковки.
Говяжья печень в кулинарии
Говяжья печень сохранит максимальное количество полезных свойств при минимальной термической обработке. Если кусочки печени внутри остались розовыми, но без крови, значит, продукт готов. Печень говяжью тушат, отваривают, жарят, из неё готовят паштеты, муссы, оладьи, котлеты и блинные пироги.
В печени много воды, поэтому она быстро портится. Перед готовкой ее надо внимательно осматривать, все вызывающее недоверие нещадно уничтожать.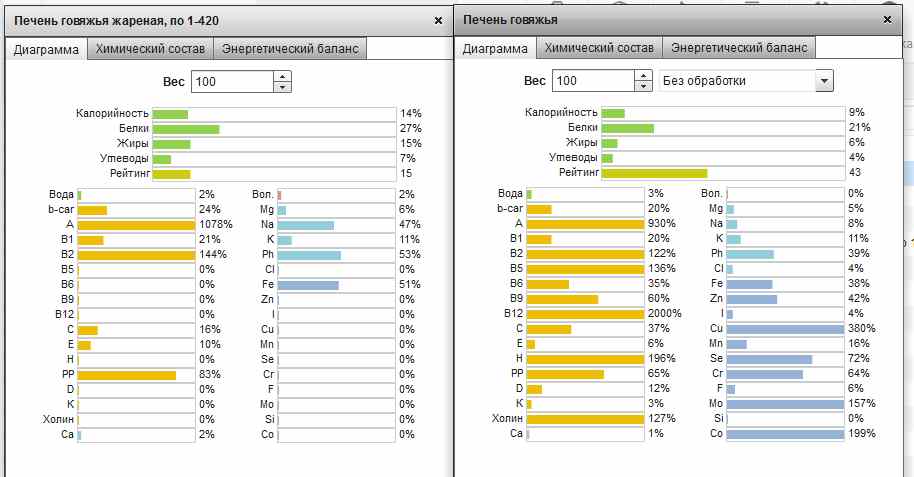 Печень получится особенно нежной, если перед приготовлением её подержать некоторое время в молоке. Лишних две-три минуты обжарки говяжьей печени портят вкус и делают её жёсткой и сухой. Перед тепловой обработкой печень необходимо освободить от желчных протоков и пленки и тщательно промыть.
Печень получится особенно нежной, если перед приготовлением её подержать некоторое время в молоке. Лишних две-три минуты обжарки говяжьей печени портят вкус и делают её жёсткой и сухой. Перед тепловой обработкой печень необходимо освободить от желчных протоков и пленки и тщательно промыть.
Некоторые хитрости приготовления говяжьей печени, необычные рецепты и полезные советы можно найти в нашей статье Как приготовить печень говяжью.
Больше о говяжьей печени, о её пользе и вреде смотрите в видеоролике «Говяжья печень. Фабрика плюсов» телепрограммы «Жить здорово!».
Специально для Calorizator.ru
Копирование данной статьи целиком или частично запрещено.
Печень говяжья – один из употребляемых в пищу внутренних органов крупного рогатого скота. В 100 граммах говяжьей печени содержится около 130 ккал. СоставХимический состав говяжьей печени отличается повышенным содержанием воды, белков, жира, углеводов, витаминов (A, B1, B2, C, E), макро- (калий, кальций, натрий, магний, фосфор) и микроэлементов (железо, йод, марганец, медь, селен, хром, фтор, цинк). Как готовитьЗначительная пищевая ценность, относительная безопасность для здоровья, а также привлекательный вкус и аромат сделали говяжью печень одним из самых популярных пищевых продуктов. Легкость в приготовлении позволяют использовать разнообразные методы кулинарной обработки. Но при этом следует учитывать ряд нюансов, связанных со специфическими особенностями говяжьей печени. Прежде всего, это длительность тепловой обработки, в особенности при обжаривании. Чрезмерно длительное тепловое воздействие негативно сказывается не только на пищевой ценности данной разновидности субпродуктов, но и на органолептических свойствах – говяжья печень становится излишне жесткой и практически безвкусной. Кроме того, она при приготовлении способна принимать на себя ароматы других пищевых продуктов. Именно поэтому при приготовлении блюд из говяжьей печени рекомендуется использовать различные ингредиенты с интенсивным вкусом и ароматом, начиная от обычной зелени и заканчивая различными фруктами. Блюда из говяжьей печени подают, как отдельно, так и вместе с гарнирами, в качестве которых лучше всего использовать жареные, отварные и тушеные овощи, а также крупы или макаронные изделия. В качестве дополнения рекомендуются хлебобулочные изделия, острые соусы. С чем сочетаетсяГовяжья печень превосходно сочетается с большинством популярных пищевых продуктов, в особенности с овощами, грибами, кисломолочной продукцией, крупяными и макаронными изделиями, некоторыми фруктами. Как выбиратьПри выборе говяжьей печени следует ориентироваться, прежде всего, на ее внешний облик. Качественные субпродукты данного вида отличаются плотной и упругой консистенцией, гладкой поверхностью, равномерно окрашенной в темные оттенки красно-коричневого цвета, а также отсутствием желчного пузыря с протоками и наружных кровеносных сосудов и лимфоузлов. ХранениеТо, что говяжья печень представлена в продаже, будучи замороженной, объяснить достаточно просто. Химический состав говяжьей печени представляет собой внушительный перечень разнообразных биологически активных веществ, большинство из которых имеет жизненно важное значение в рационе питания человека. В частности, блюда из этого субпродукта стимулируют процессы кроветворения и метаболизма, препятствуют возникновению ряда заболеваний почек, сердечно-сосудистой, пищеварительной и центральной нервной системы. Кроме того, говяжья печень обеспечивает эффективную защиту от вредного воздействия табака и алкоголя, улучшает состояние костных и мышечных тканей, нормализует свертываемость крови, оказывает антиоксидантное, противовоспалительное и иммуностимулирующее воздействие. Индивидуальная непереносимость, повышенный уровень холестерина, пожилой возраст (употреблять с осторожностью), хронические и недавно перенесенные заболевания сердечно-сосудистой системы (инфаркт миокарда, инсульт, стенокардия, тромбоз), высокая вероятность содержания в печени опасных для здоровья веществ, необходимость в обязательной тепловой обработке перед употреблением в пищу. Печень говяжья: состав, калорийность и пищевая ценность на 100 г
Общая информация Вода 70,81 г Энергетическая ценность 135 ккал Энергия 564 кДж Белки 20,36 г Жиры 3,63 г Неорганические вещества 1,31 г Углеводы 3,89 г Минералы Кальций, Ca 5 мг Железо, Fe 4,9 мг Магний, Mg 18 мг Фосфор, P 387 мг Калий, K 313 мг Натрий, Na 69 мг Цинк, Zn 4 мг Медь, Cu 9,755 мг Марганец, Mn 0,31 мг Селен, Se 39,7 мкг Витамины Витамин С 1,3 мг Тиамин 0,189 мг Рибофлавин 2,755 мг Никотиновая кислота 13,175 мг Пантотеновая кислота 7,173 мг Витамин B-6 1,083 мг Фолаты, всего 290 мкг Фолиевая кислота, пищевая 290 мкг Фолиевая кислота, DFE 290 мкг Холин, всего 333,3 мг Бетаин 4,4 мг Витамин B-12 59,3 мкг Витамин A, RAE 4968 мкг Ретинол 4948 мкг Каротин, бета- 232 мкг Каротин, альфа 11 мкг Криптоксантин, бета 13 мкг Витамин A, IU 16898 МЕ Витамин Е (альфа-токоферол) 0,38 мг Токоферол, гамма 0,07 мг Витамин D (D2 + D3) 1,2 мкг Витамин D3 (холекальциферол) 1,2 мкг Витамин D 49 МЕ Витамин К (филлохинон) 3,1 мкг Липиды Жирные кислоты, насыщенные 1,233 г 14:0 0,015 г 15:0 0,007 г 16:0 0,312 г 17:0 0,03 г 18:0 0,862 г 22:0 0,009 г Жирные кислоты, мононенасыщенные 0,479 г 16:1 недифференцированно 0,036 г 17:1 0,013 г 18:1 недифференцированно 0,423 г 20:1 0,007 г Жирные кислоты, полиненасыщенные 0,465 г 18:2 недифференцировано 0,299 г 18:2 n-6 c,c 0,299 г 18:3 недифференцированно 0,016 г 18:3 n-3 c,c,c (ALA) 0,007 г 18:3 n-6 c,c,c 0,009 г 20:2 n-6 c,c 0,01 г 20:4 недифференцированно 0,141 г Жирные кислоты, всего транс 0,17 г Холестерин 275 мг Аминокислоты Триптофан 0,263 г Треонин 0,869 г Изолейцин 0,967 г Лейцин 1,91 г Лизин 1,607 г Метионин 0,543 г Цистин 0,376 г Фенилаланин 1,084 г Тирозин 0,807 г Валин 1,26 г Аргинин 1,241 г Гистидин 0,629 г Аланин 1,164 г Аспарагиновая кислота 1,927 г Глутаминовая кислота 2,612 г Глицин 1,164 г Пролин 0,961 г Серин 0,905 г Гидроксипролин 0,046 г | Оригинальные рецепты с фото: |
польза и вред, состав и противопоказания.
 Калорийность говяжьей печени
Калорийность говяжьей печениПолезные свойства
Хотя польза печени доказана научно, до сих пор можно столкнуться с народным мнением, что этот субпродукт вреден из-за того, что является естественным фильтром, собирает в себе все токсичные вещества, которые попадают в организм животного. Это верно только в том случае, если питание было несбалансированным, и корма содержали химические компоненты. Если животное выращивается в экологически чистой обстановке, его печень также чиста и очень полезна.
Полезные свойства говяжьей печени известны уже на протяжении многих веков. Ещё Авиценна рекомендовал своим пациентам ее сок, чтобы улучшить зрение. Хорошо было известно еще до нашей эры положительное влияние продукта на состав крови.
Позитивное воздействие на здоровье объясняется химическим составом. Это кладезь витаминов, аминокислот и минералов, к тому же они очень хорошо усваиваются. Очень высока в составе концентрация витаминов группы В и аскорбиновой кислоты.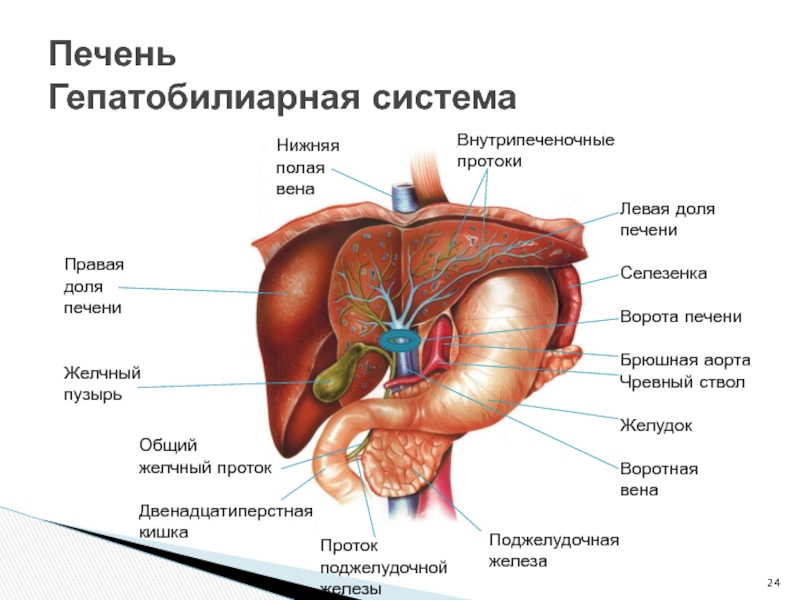 Содержание гемового железа позволяет рекомендовать продукт людям с анемией, нарушением выработки гемоглобина. К тому же содержание меди и витамина С позволяет его лучше усваивать.
Содержание гемового железа позволяет рекомендовать продукт людям с анемией, нарушением выработки гемоглобина. К тому же содержание меди и витамина С позволяет его лучше усваивать.
Главный витамин говяжьей печени — А, поэтому сам продукт еще называют депо по его хранению. Регулярное употребление блюд из этого субпродукта действительно способствует улучшению зрения, работы сердечно-сосудистой системы, почек и нервной системы. Постепенно улучшается состояние ногтей и волос, кожные покровы приобретают гладкость и здоровый цвет.
Очень важен в составе печени витамин B12, который содержится только в животных продуктах, здесь его концентрация наиболее высока.
Антиоксидант тиамин защищает организм от вредных воздействий алкоголя и табака, улучшает работу мозга. Гепарин и хром повышают свертываемость крови, поэтому печень рекомендуют больным тромбозом, атеросклерозом и другими сосудистыми заболеваниями. Кальций, витамины С и D укрепляют опорно-двигательный аппарат, облегчают течение остеопороза.
Гепарин и хром повышают свертываемость крови, поэтому печень рекомендуют больным тромбозом, атеросклерозом и другими сосудистыми заболеваниями. Кальций, витамины С и D укрепляют опорно-двигательный аппарат, облегчают течение остеопороза.
Печень полезна при физических нагрузках, так как повышает устойчивость к ним благодаря содержанию кератина, ускоряющего протекание метаболических процессов. Фолиевая кислота (витамин В9) укрепляет иммунитет, а у беременных способствует полноценному развитию плода.
Печень говяжья при диете
В диетическом питании говяжья печень является одним из самых часто используемых продуктов. Как видно из вышесказанного, она облегчает течение многих болезней и укрепляет иммунитет. Также ее включают в спортивные диеты, чтобы организм получал в достаточных количествах все микроэлементы и витамины.
Продукт незаменим в диетах для нормализации веса. Есть даже отдельная печеночная диета, которая при ожирении позволяет сбрасывать до 8 кг в неделю. Это связано с низкой калорийностью продукта и одновременной способностью вызывать чувство насыщения. А то, что при такой диете активизируется метаболизм, позволяет нормализовать обменные процессы: из организма быстрее выводятся токсичные соединения, он избавляется от лишних килограммов.
Это связано с низкой калорийностью продукта и одновременной способностью вызывать чувство насыщения. А то, что при такой диете активизируется метаболизм, позволяет нормализовать обменные процессы: из организма быстрее выводятся токсичные соединения, он избавляется от лишних килограммов.
Печень: анатомия и функции | Johns Hopkins Medicine
Анатомия печени
Печень расположена в верхней правой части брюшной полости, под диафрагмой, над желудком, правой почкой и кишечником.
Печень имеет форму конуса и представляет собой темно-красновато-коричневый орган, который весит около 3 фунтов.
Есть 2 различных источника, которые снабжают печень кровью, включая следующие:
В печени в любой момент находится около одной пинты (13%) кровоснабжения организма.Печень состоит из 2-х основных долей. Оба состоят из 8 сегментов, состоящих из 1000 долек (маленьких долей). Эти дольки соединены с небольшими протоками (трубками), которые соединяются с более крупными протоками, образуя общий печеночный проток. Общий печеночный проток транспортирует желчь, вырабатываемую клетками печени, в желчный пузырь и двенадцатиперстную кишку (первая часть тонкой кишки) через общий желчный проток.
Общий печеночный проток транспортирует желчь, вырабатываемую клетками печени, в желчный пузырь и двенадцатиперстную кишку (первая часть тонкой кишки) через общий желчный проток.
Функции печени
Печень регулирует большинство химических уровней в крови и выделяет продукт, называемый желчью.Это помогает выводить продукты жизнедеятельности из печени. Вся кровь, покидающая желудок и кишечник, проходит через печень. Печень обрабатывает эту кровь и расщепляет, уравновешивает и создает питательные вещества, а также метаболизирует лекарства в формы, которые легче использовать для остального тела или которые нетоксичны. С печенью идентифицировано более 500 жизненно важных функций. Вот некоторые из наиболее известных функций:
Производство желчи, которая помогает уносить отходы и расщеплять жиры в тонком кишечнике во время пищеварения
Производство определенных белков для плазмы крови
Производство холестерина и специальных белков, помогающих переносить жиры через тело
Преобразование избыточной глюкозы в гликоген для хранения (позже гликоген может быть преобразован обратно в глюкозу для получения энергии), а также для баланса и выработки глюкозы по мере необходимости
Регулирование уровня аминокислот в крови, которые образуют строительные блоки белков
Обработка гемоглобина для использования в нем железа (печень хранит железо)
Превращение ядовитого аммиака в мочевину (мочевина является конечным продуктом белкового обмена и выводится с мочой)
Очистка крови от наркотиков и других ядовитых веществ
Регулирование свертывания крови
Противодействие инфекциям за счет создания иммунных факторов и удаления бактерий из кровотока
Удаление билирубина, также из красных кровяных телец.
 При скоплении билирубина кожа и глаза желтеют.
При скоплении билирубина кожа и глаза желтеют.
Когда печень расщепляет вредные вещества, ее побочные продукты выделяются с желчью или кровью. Побочные продукты желчи попадают в кишечник и покидают организм в виде кала. Побочные продукты крови отфильтровываются почками и покидают организм в виде мочи.
Печень | Безграничная анатомия и физиология
Печень
Печень вырабатывает желчь, которая необходима для переваривания жиров.
Цели обучения
Обобщить роль печени в пищеварении
Основные выводы
Ключевые моменты
- Печень – жизненно важный орган с широким спектром функций, включая детоксикацию, синтез белка и производство желчи, необходимой для пищеварения.
- Желчь, вырабатываемая печенью, необходима для переваривания жиров. Желчь образуется в печени и либо накапливается в желчном пузыре, либо выделяется непосредственно в тонкий кишечник.
Ключевые термины
- печень : большой орган в организме, который накапливает и метаболизирует питательные вещества, разрушает токсины и производит желчь.
 Он отвечает за тысячи биохимических реакций.
Он отвечает за тысячи биохимических реакций. - желчь : горький, коричневато-желтый или зеленовато-желтый секрет, вырабатываемый печенью, накапливающийся в желчном пузыре и выделяемый в двенадцатиперстную кишку, где он помогает процессу пищеварения.
Роль печени
Печень обычно весит от 1 до 1 кг.3—3,0 кг, представляет собой мягкий орган розовато-коричневого цвета. Это второй по величине орган в организме, расположенный на правой стороне живота.
Печень человека : Фотография недавно удаленной печени человека.
Печень играет важную роль в метаболизме и выполняет ряд функций в организме, включая хранение гликогена, синтез белков плазмы и детоксикацию лекарств. Он также производит желчь, которая важна для пищеварения.
Печень снабжена двумя основными кровеносными сосудами в ее правой доле: печеночной артерией и воротной веной.По воротной вене венозная кровь поступает из селезенки, поджелудочной железы и тонкого кишечника, чтобы печень могла перерабатывать питательные вещества и побочные продукты переваривания пищи.
Желчь
Желчь, вырабатываемая в печени, необходима для переваривания жиров. Желчь образуется в печени и накапливается в желчном пузыре или выделяется непосредственно в тонкий кишечник. После накопления в желчном пузыре желчь становится более концентрированной, чем когда она покидает печень; это увеличивает его эффективность и усиливает его действие на переваривание жиров.
Анатомия печени
Печень расположена в брюшной полости и имеет четыре доли.
Цели обучения
Деталь анатомии печени
Основные выводы
Ключевые моменты
- Печень человека обычно весит 1,44–1,66 кг (3,2–3,7 фунта) и представляет собой мягкий розовато-коричневый треугольный орган.
- Печень является одновременно самым большим внутренним органом (самым большим органом в целом является кожа) и самой большой железой в организме человека.
- Печень связана с двумя крупными кровеносными сосудами: печеночной артерией и воротной веной.

- Традиционно печень делится на четыре доли: левую, правую, хвостатую и квадратную. Доли делятся на дольки, функциональные единицы печени.
- Каждая долька состоит из миллионов печеночных клеток, которые являются основными метаболическими клетками печени.
Ключевые термины
- долька : подразделение четырех основных долей печени, основной функциональной единицы печени.
Печень
Печень человека является одновременно самым большим внутренним органом (самым большим органом в целом является кожа) и самой большой железой в человеческом теле. Это мягкий розовато-коричневый треугольный орган, обычно весящий 1,44–1,66 кг (3,2–3,7 фунта).
Печень выполняет широкий спектр функций, включая детоксикацию, синтез белка и производство биохимических веществ, необходимых для пищеварения. Он расположен в правом верхнем квадранте брюшной полости, чуть ниже диафрагмы.Печень находится справа от желудка и покрывает желчный пузырь.
Положение печени : пространственное соотношение между печенью, желудком, желчным пузырем и поджелудочной железой. Печень видна над желудком, желчным пузырем и поджелудочной железой.
Печень связана с двумя крупными кровеносными сосудами, печеночной артерией и воротной веной. Печеночная артерия переносит кровь из аорты в печень, тогда как воротная вена переносит кровь, содержащую переваренные питательные вещества, из всего желудочно-кишечного тракта, а также из селезенки и поджелудочной железы в печень.Эти кровеносные сосуды делятся на капилляры, которые затем переходят в дольку.
Доли печени
Традиционно печень делится на четыре доли: левую, правую, хвостатую и квадратную. Доли делятся на дольки, функциональные единицы печени. Каждая долька состоит из миллионов печеночных клеток, которые являются основными метаболическими клетками печени.
Гистология печени
Гепатоциты – это основные тканевые клетки печени. Желчный пузырь содержит слизистую оболочку, мышечный, перимускулярный и серозный слои.
Желчный пузырь содержит слизистую оболочку, мышечный, перимускулярный и серозный слои.
Цели обучения
Опишите гистологию печени
Основные выводы
Ключевые моменты
- Гепатоцит является основной тканевой клеткой печени и составляет 70–80% цитоплазматической массы печени.
- Гепатоциты содержат большое количество шероховатой эндоплазматической сети и свободных рибосом.
- Гепатоциты участвуют в: синтезе белков; хранение белка; превращение углеводов; синтез холестерина, солей желчных кислот и фосфолипидов; и детоксикация, модификация и выведение экзогенных и эндогенных веществ.
- Гепатоциты уникальны тем, что они являются одним из немногих типов клеток человеческого тела, которые способны к регенерации.
- Желчный пузырь состоит из нескольких слоев: слизистой оболочки (эпителий и собственная пластинка), мышечной, перимускулярной и серозной.
Ключевые термины
- гепатоцит : Любая из клеток печени, отвечающая за метаболизм белков, углеводов и липидов, а также за детоксикацию.

Печень
Гепатоциты : поперечный разрез печени человека, на котором видны гепатоциты.
Гепатоцит является основной тканевой клеткой печени и составляет 70–80% цитоплазматической массы печени. Гепатоциты содержат большое количество грубого эндоплазматического ретикулума и свободных рибосом. Гепатоциты участвуют в:
- Синтез белков.
- Хранение протеина.
- Превращение углеводов.
- Синтез холестерина, солей желчных кислот и фосфолипидов.
- Детоксикация, модификация и выведение экзогенных и эндогенных веществ.
Гепатоциты также инициируют образование и секрецию желчи. Гепатоциты организованы в пластинки, разделенные сосудистыми каналами (синусоидами) для кровеносных сосудов. Пластинки гепатоцитов у млекопитающих имеют толщину в одну клетку.
Гепатоциты уникальны тем, что они являются одним из немногих типов клеток человеческого тела, способных к регенерации. Гепатоциты происходят из гепатобластов, стволовых клеток-предшественников печени, которые делятся с образованием новых гепатоцитов. Печень способна к полной регенерации всего лишь из 25% исходного органа.
Печень способна к полной регенерации всего лишь из 25% исходного органа.
Кровоснабжение печени
В портальной системе печени печень получает двойное кровоснабжение от воротной вены печени и печеночных артерий.
Цели обучения
Обозначьте кровоток к печени и от нее
Основные выводы
Ключевые моменты
- Печеночная воротная вена снабжает печень 75% крови, а печеночные артерии – оставшимися 25%.
- Примерно половина потребности печени в кислороде удовлетворяется воротной веной печени, а половина – печеночными артериями.
- Печеночная портальная система соединяет капилляры желудочно-кишечного тракта с капиллярами печени. Богатая питательными веществами кровь покидает желудочно-кишечный тракт и сначала попадает в печень для обработки, а затем направляется в сердце.
Ключевые термины
- печеночные артерии : кровеносный сосуд, который поставляет насыщенную кислородом кровь в печень.

- воротная вена печени : сосуд, расположенный в брюшной полости, который образован слиянием верхней брыжеечной и селезеночной вен, которые направляют кровь из желудочно-кишечного тракта и селезенки в капиллярные русла в печени.
- Кофакторы : Вещество, особенно кофермент или металл, которое должно присутствовать для функционирования фермента.
В портальной системе печени печень получает двойное кровоснабжение от воротной вены печени и печеночных артерий.По воротной вене печени проходит венозная кровь, оттекающая из селезенки, желудочно-кишечного тракта и связанных с ним органов; он снабжает печень примерно 75% крови. Печеночные артерии снабжают печень артериальной кровью и обеспечивают оставшуюся часть ее кровотока.
Кислород поступает из обоих источников; Примерно половина потребности печени в кислороде удовлетворяется воротной веной печени, а половина – печеночными артериями. Кровь течет через ткань печени и впадает в центральную вену каждой дольки. Центральные вены сливаются в печеночные вены, которые собирают кровь, покидающую печень, и доставляют ее к сердцу.
Центральные вены сливаются в печеночные вены, которые собирают кровь, покидающую печень, и доставляют ее к сердцу.
Печеночные вены : изображение печени с маркированными печеночными венами. Они расположены в нижней полой вене.
Портальная система – это венозная структура, которая позволяет крови из одного набора капиллярных русел стекать в другой набор капиллярных русел, не возвращая эту кровь сначала в сердце. Большинство капилляров в организме впадают непосредственно в сердце, поэтому портальные системы необычны.
Печеночная портальная система соединяет капилляры желудочно-кишечного тракта с капиллярами печени. Богатая питательными веществами кровь покидает желудочно-кишечный тракт и сначала попадает в печень для обработки, а затем направляется в сердце. Здесь углеводы и аминокислоты могут храниться или использоваться для производства новых белков и углеводов.
Печень также удаляет витамины и кофакторы из крови для хранения, а также фильтрует любые токсины, которые могли быть поглощены вместе с пищей. Когда любое из этих накопленных веществ необходимо, печень возвращает их в циркуляцию через печеночные вены.
Когда любое из этих накопленных веществ необходимо, печень возвращает их в циркуляцию через печеночные вены.
Циркуляция воротной вены печени : Схема, на которой показана воротная вена печени и ее территория.
Функция печени
Считается, что печень отвечает за 500 отдельных функций.
Цели обучения
Перечислить некоторые функции печени
Основные выводы
Ключевые моменты
- Считается, что печень отвечает за 500 отдельных функций, обычно в сочетании с другими системами и органами.
- Различные функции печени выполняются клетками печени или гепатоцитами.
- Чрезмерное употребление алкоголя может вызвать заболевание печени.
- Ткань печени алкоголика может забиваться жирами и отрицательно влиять на функцию печени.
Ключевые термины
- Заболевание печени : Также называется заболеванием печени, это общий термин, относящийся к повреждению или заболеванию печени.

- IGF : гормон, сходный по молекулярной структуре с инсулином.Он играет важную роль в детском росте и продолжает оказывать анаболическое действие на взрослых. Синтетический аналог IGF-1, меказермин, используется для лечения нарушения роста.
Функции печени
Считается, что человеческая печень отвечает за 500 отдельных функций, обычно в сочетании с другими системами и органами. Различные функции печени выполняются клетками печени или гепатоцитами. В настоящее время не существует искусственного органа или устройства, способного имитировать все функции печени.
Печень : печень, или гепар, является жизненно важным органом, присутствующим у позвоночных и некоторых других животных. Он выполняет широкий спектр функций, включая детоксикацию, синтез белка и производство биохимических веществ, необходимых для пищеварения.
Печень – это опора белкового обмена: она не только синтезирует, но и разрушает. Он выполняет несколько ролей в метаболизме углеводов и липидов. Основная масса липопротеинов синтезируется в печени.
Основная масса липопротеинов синтезируется в печени.
Ткань печени алкоголика : здоровая печень может расщеплять алкоголь.Однако перегруженная печень алкоголика может забиваться жирами, что отрицательно сказывается на ее функции. Этот тип ткани чаще всего встречается при алкогольном гепатите (распространенность 65%) и алкогольном циррозе печени (распространенность 51%).
В первом триместре плода печень является основным местом производства красных кровяных телец. К 32 неделе беременности костный мозг почти полностью взял на себя эту задачу.
Печень также производит инсулиноподобный фактор роста 1 (IGF-1), полипептидный белковый гормон, который играет важную роль в детском росте и продолжает оказывать анаболическое действие у взрослых.
Печень хранит множество веществ, включая глюкозу (в форме гликогена), витамин A (запасы на 1-2 года), витамин D (запасы на 1-4 месяца), витамин B12 (запасы на 1-3 года). ), железо и медь. Печень отвечает за иммунологические эффекты, действуя как сито для антигенов, которые переносятся к ней через портальную систему.
Печень синтезирует ангиотензиноген, гормон, который отвечает за повышение кровяного давления, когда ангиотензиноген активируется ренином, ферментом, который высвобождается, когда почки ощущают низкое кровяное давление.
Печень расщепляет или изменяет токсичные вещества, такие как алкоголь и большинство лекарственных средств, в процессе, называемом метаболизмом лекарств. Иногда это приводит к отравлению, когда метаболит более токсичен, чем его предшественник.
Предпочтительно, чтобы токсины были конъюгированы, чтобы способствовать их выведению с желчью или мочой. Печень расщепляет инсулин и другие гормоны.
Желчь
Желчь – это жидкость, вырабатываемая печенью, которая помогает процессу пищеварения и всасыванию липидов в тонком кишечнике.
Цели обучения
Обобщить состав и функцию желчи
Основные выводы
Ключевые моменты
- Желчь – это композиция из следующих материалов: воды (85%), желчных солей (10%), слизи и пигментов (3%), жиров (1%), неорганических солей (0,7%) и холестерина (0,3%). ).
- Желчь может стекать непосредственно в двенадцатиперстную кишку или временно накапливаться в желчном пузыре.
- Щелочная желчь также нейтрализует избыток желудочной кислоты в тонком кишечнике.
Ключевые термины
- желчь : горький, коричневато-желтый или зеленовато-желтый секрет, вырабатываемый печенью, накапливающийся в желчном пузыре и выделяемый в двенадцатиперстную кишку, где он помогает процессу пищеварения.
Желчь : Микрофотография желчи (желтый материал) при биопсии печени.
Желчь или желчь – это горьковатая жидкость от темно-зеленого до желтовато-коричневого цвета, вырабатываемая печенью и помогающая процессу переваривания липидов в тонком кишечнике.Желчь хранится в желчном пузыре и после еды выводится в двенадцатиперстную кишку через желчный проток. Желчь состоит из следующих материалов: воды (85%), желчных солей (10%), слизи и пигментов (3%), жиров (1%), неорганических солей (0,7%) и холестерина (0,3%).
Желчь действует как поверхностно-активное вещество, помогая эмульгировать жиры в пище, так же, как мыло эмульгирует жир. Соли желчных кислот являются ионно заряженными, с гидрофобным концом и гидрофильным концом.
При контакте с водой, смешанной с жиром, например, в тонком кишечнике, соли желчных кислот собираются вокруг жировой капли, причем их гидрофобная сторона направлена в сторону жира, а их гидрофильная сторона – в сторону воды.Это увеличивает площадь поверхности жира и обеспечивает больший доступ ферментов поджелудочной железы, которые расщепляют жиры.
Поскольку желчь увеличивает всасывание жиров, она играет важную роль в усвоении жирорастворимых витаминов, таких как витамины D, E, K и A.
Помимо пищеварительной функции, желчь служит также путем выведения билирубина, побочного продукта эритроцитов, который перерабатывается печенью. Щелочная желчь также нейтрализует избыток желудочной кислоты, прежде чем она попадет в подвздошную кишку, последний отдел тонкой кишки.
Соли желчных кислот также действуют как бактерициды, уничтожая многие микробы, которые могут присутствовать в пище.
Действие солей желчных кислот на липиды : соли желчных кислот собираются вокруг жира и разделяют их на маленькие капельки, называемые мицеллами.
Печень | анатомия | Britannica
Печень , самая большая железа в организме, губчатая масса клиновидных долей, которая выполняет множество метаболических и секреторных функций. Печень выделяет желчь, пищеварительную жидкость; метаболизирует белки, углеводы и жиры; хранит гликоген, витамины и другие вещества; синтезирует факторы свертывания крови; удаляет шлаки и токсичные вещества из крови; регулирует объем крови; и разрушает старые эритроциты.
Ткань печени состоит из массы клеток, через которые проходят желчные протоки и кровеносные сосуды. Клетки печени составляют около 60 процентов ткани и выполняют больше метаболических функций, чем любая другая группа клеток в организме. Вторая группа клеток, называемая клетками Купфера, выстилает мельчайшие каналы сосудистой системы печени и играет роль в кроветворении, выработке антител и попадании в организм чужеродных частиц и клеточного мусора.
печень человекаВид печени спереди и сзади.
Британская энциклопедия, Inc.Британская викторина
Что скрывается под кожей: тест по анатомии человека
Человеческое тело состоит из множества различных систем, работающих вместе, чтобы создать удивительную машину. Вы знаете, из чего сделано ваше тело? Пройдите нашу викторину по анатомии человека и узнайте.
Ежедневно печень выделяет от 800 до 1000 мл (около 1 литра) желчи, которая содержит соли желчных кислот, необходимые для переваривания жиров, содержащихся в пище. Желчь также является средой для выведения некоторых продуктов метаболизма, лекарств и токсичных веществ. Из печени по системе протоков желчь переносится в общий желчный проток, который впадает в двенадцатиперстную кишку тонкой кишки и соединяется с желчным пузырем, где она концентрируется и хранится. Наличие жира в двенадцатиперстной кишке стимулирует отток желчи из желчного пузыря в тонкий кишечник.Старые (изношенные) эритроциты разрушаются в печени, селезенке и костном мозге. Пигмент билирубин, образующийся в процессе распада гемоглобина, выделяется с желчью, придавая ей характерный зеленовато-оранжевый цвет, и выводится из организма через кишечник.
Клетки печени синтезируют ряд ферментов. Поскольку кровь течет через печень как из воротной вены, так и из печеночной артерии, клетки и ферменты фильтруются. Питательные вещества, поступающие в печень из кишечника, преобразуются в формы, которые могут использоваться клетками организма или сохраняются для будущего использования.Жиры превращаются в жирные кислоты, а затем в углеводы или кетоновые тела и транспортируются кровью в ткани, где они метаболизируются. Сахар превращается в гликоген, который остается в печени до тех пор, пока он не понадобится для производства энергии; затем он снова превращается в глюкозу и попадает в кровоток. Печень производит белки сыворотки крови, включая альбумин и несколько факторов свертывания, и поставляет их в кровь. Печень также метаболизирует азотсодержащие продукты жизнедеятельности и выводит токсичные вещества, подготавливая их к выведению с мочой или калом.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчасРаспространенным признаком нарушения функции печени является желтуха, желтушность глаз и кожи, возникающая из-за чрезмерного содержания билирубина в крови. Желтуха может быть результатом аномально высокого уровня разрушения эритроцитов (гемолитическая желтуха), недостаточного поглощения или транспорта билирубина клетками печени (гепатоцеллюлярная желтуха) или закупорки системы желчных протоков (механическая желтуха). Неспособность клеток печени функционировать может быть результатом гепатита, цирроза, опухолей, обструкции сосудов или отравления.Симптомы могут включать слабость, низкое кровяное давление, легкие кровоподтеки и кровотечения, тремор и скопление жидкости в брюшной полости. Анализы крови могут выявить аномальные уровни билирубина, холестерина, белков сыворотки, мочевины, аммиака и различных ферментов. Конкретный диагноз проблемы с печенью может быть установлен путем выполнения пункционной биопсии.
микроскопическая структура печени человекаКлетки печени или гепатоциты имеют прямой доступ к кровоснабжению печени через небольшие капилляры, называемые синусоидами.Гепатоциты выполняют множество метаболических функций, включая производство желчи. Клетки Купфера выстилают сосудистую систему печени; они играют роль в кроветворении и разрушении клеточного мусора.
Британская энциклопедия, Inc.Печень подвержена множеству других расстройств и заболеваний. Абсцессы могут быть вызваны острым аппендицитом; те, которые возникают в желчных протоках, могут возникать в результате образования камней в желчном пузыре или после хирургического вмешательства. Паразит, вызывающий амебную дизентерию в тропиках, также может вызывать абсцессы печени.Различные другие паразиты, распространенные в разных частях мира, также поражают печень. Рак печени является распространенным явлением, чаще всего возникающим в виде вторичных опухолей, возникающих в других частях тела. Заболевания накопления гликогена, группа наследственных заболеваний, вызывают накопление гликогена в печени и недостаточное поступление глюкозы в кровь. Некоторые лекарства могут повредить печень, вызывая желтуху.
Структурные и функциональные аспекты печени и синусоидальных клеток печени в связи с метастазами карциномы толстой кишки
Печень является преобладающим местом рецидива заболевания после первоначальной терапевтической операции на толстой кишке, в основном из-за двух факторов.Во-первых, жизнеспособные опухолевые клетки могут выходить в портальный кровоток во время хирургических манипуляций и проникать в печень [41]. Во-вторых, серьезное хирургическое вмешательство вызывает временное послеоперационное ослабление иммунной системы [42–44]. Таким образом, временная иммуносупрессия, вызванная хирургическим вмешательством, связана с повышенным риском метастазирования. Когда рак толстой кишки распространяется на печень, удаление метастазов с помощью хирургической резекции, криотерапии или радиочастоты является единственным лечебным лечением [45]. Более того, подавляющее большинство пациентов не поддаются хирургической резекции из-за наличия множественных метастазов.Для разработки новых стратегий, направленных на предотвращение метастазирования, крайне важно понимать механизмы клеточной защиты от опухолевых клеток и механизмы ускользания от опухоли.
Цитотоксичность синусоидальных клеток по отношению к опухолевым клеткам
Когда опухолевые клетки проникают в сосудистое русло и метастазируют в печень, они сталкиваются с защитными механизмами, специфичными для печени. Клетки Купфера и NK-клетки печени являются основными резидентными клетками иммунного надзора, но синусоидальные эндотелиальные клетки также участвуют в этом процессе.
Клетки Купфера Самая важная функция клеток Купфера – защита от инфекций и опухолевых клеток. Клетки Купфера действуют как антигенпрезентирующие клетки и как эффекторные клетки, которые действуют непосредственно путем фагоцитоза или косвенно путем активации других клеток, например NK-клетки [46,47]. Хотя клетки Купфера постоянно действуют как мусорщики, они могут активироваться разными путями. Во-первых, их активацию могут запускать растворимые медиаторы. IFN-γ – это типичный фактор активации макрофагов.Он играет центральную роль в развитии иммунных ответов с преобладанием Th2 и влияет не только на макрофаги аутокринным образом, но и на другие иммунные клетки.
Одним из ключевых событий во время реакций врожденного иммунитета является продукция IL-12, в основном макрофагами [48]. IL-12 побуждает NK-клетки быстро секретировать IFN-γ, который, в свою очередь, активирует макрофаги на ранней стадии иммунного ответа. Он также индуцирует продукцию IFN-γ Т-клетками. IL-18, который продуцируется клетками Купфера и другими типами клеток, также участвует в усилении продукции IFN-γ Т-клетками [49,50].Макрофаги также секретируют IFN-γ при одновременной стимуляции IL-12 и IL-18. Известно, что IFN-γ является возможным редуктором метастазирования рака толстой кишки в печень [51].
Макрофаги также могут быть активированы путем прямого взаимодействия с микроорганизмами или бактериальными продуктами, такими как липополисахарид, глюкан, мурамилдипептид и липид A [52]. Ключевая роль IFN-γ в клиренсе различных внутриклеточных патогенов была подробно продемонстрирована [53,54]. Было описано, что макрофаги выделяют цитотоксический радикал NO [55,56]. Исследования in vitro показали, что NO вызывает митохондриальную дисфункцию в опухолевых клетках, за которой следует дисфункция мембранного барьера в синусоиде печени [57,58]. Другим важным цитотоксическим фактором, высвобождаемым активированными макрофагами, является фактор некроза опухоли альфа (TNF-α), который продуцируется как в растворимой, так и в мембраносвязанной формах. После связывания с его рецептором в клетке-мишени может быть индуцирован апоптоз [59].
Цитотоксичность макрофагов можно разделить на антителозависимую и антителозависимую цитотоксичность, опосредованную клетками.Оба пути зависят от контакта и вызывают гибель опухолевых клеток через несколько часов. Антителозависимая клеточно-опосредованная цитотоксичность основана на распознавании покрытой антителом мишени рецепторами Fc на эффекторных клетках [60-62]. При перекрестном связывании рецептора Fc происходит секреция цитотоксических медиаторов. Вероятно, участвует секреция активных форм кислорода, IL-1 и TNF-α [63]. Антител-независимая клеточно-опосредованная цитотоксичность включает связывание с макрофагом с последующей транслокацией лизосомных органелл к мишени [47].Более того, цитотоксичность по отношению к опухолевым мишеням включает цитолиз и фагоцитоз [64].
При определенных патофизиологических состояниях апоптоз носит хаотический и неизбирательный характер, может быть массивным и постоянно протекать в течение длительного периода времени [65]. Большое количество продуцируемых апоптотических телец фагоцитируется клетками Купфера. Недавно сообщалось, что поглощение апоптотических тел приводит к генерации лигандов смерти, таких как FasL и TNF-α на мембране клеток Купфера, но поглощение латексных шариков не вызывает подобного ответа [59].Это означает, что поглощение апоптотических тел вызывает дополнительный иммунологический ответ, включающий воспаление и фиброз печени [59,66].
Печеночные NK-клетки Цитотоксические лимфоциты (CTL) и NK-клетки вызывают гибель клеток-мишеней посредством гранул и путей, опосредованных рецепторами смерти. Апоптоз относится к организованной гибели клеток, которая необходима для поддержания гомеостаза. Характеристики апоптоза: конденсация хроматина, фрагментация ядер, образование пузырей на мембранах, сжатие клеток, деградация белка и фрагментация межнуклеосомной ДНК.Большинство морфологических изменений вызвано набором цистеиновых протеаз, которые активируются специфически в апоптотических клетках. Эти протеазы смерти гомологичны друг другу и являются членами большого семейства белков, известных как каспазы [67]. У людей было идентифицировано более десятка каспаз, и было высказано предположение, что около двух третей из них действуют при апоптозе [68,69]. Различные пути могут вызывать апоптоз, из которых наиболее известен путь Fas / FasL. Этот путь часто используется цитотоксическими Т-клетками и другими иммунокомпетентными клетками.Стимуляция рецептора Fas (CD95) лигандом Fas рекрутирует проформу инициатора каспазы 8 за счет взаимодействия с адаптерной молекулой Fas-ассоциированного домена смерти через домены смерти и эффекторные домены смерти. Это приводит к образованию комплекса, называемого сигнальным комплексом, вызывающим смерть. Затем прокаспаза 8 автокаталитически расщепляется с образованием активной инициаторной каспазы 8. Последствия активации каспазы 8 зависят от типа клетки. В клетках типа 1 другие члены семейства каспаз (например, каспаза 3) активируются напрямую [70].В клетках типа 2 активация каспазы 8 приводит к расщеплению проапоптотического члена семейства Bcl-2 Bid. Впоследствии Bid и Bax перемещаются в митохондрии, вызывая высвобождение цитохрома c . Это приводит к активации каспазы 9 за счет взаимодействия с адаптерной молекулой, активирующей апоптотический фактор протеазы. Каспаза 9 активирует каспазу 3, которая затем может выполнять свою функцию [71,72].
Гранулы CTL содержат различные белки, некоторые из которых, как известно, участвуют в гибели клеток-мишеней, такие как перфорин и гранзим.Описаны различные изоформы гранзимов. После того, как гранзим B попадает в клетку-мишень, он может непосредственно расщеплять прокаспазу 3, Bid и ингибитор каспазо-активируемой ДНКазы, тем самым вызывая апоптоз [71,73-75]. Смерть, вызванная гранзимом A, по-видимому, не зависит от путей, используемых гранзимом B [75,76]. Гранзим А не активирует каспазы в клетках-мишенях и не индуцирует расщепление других субстратов гранзима В. Функции других изоформ гранзима остаются неясными [76]. Перфорин образует трансмембранные поры и является важным активатором гранзим-опосредованного апоптоза [77].
Синусоидальные эндотелиальные клетки печени LSEC, как и клетки Купфера, экспрессируют рецептор Fc, который может участвовать в иммунологической защите. Было показано, что опосредованное FcR поглощение IgG-иммунного комплекса усиливает презентацию антигенов MHC класса II [78]. Этот процесс может происходить в компартменте, напоминающем мультивезикулярные компартменты, наблюдаемые в LSEC. Следовательно, возможно, что эти органеллы участвуют в процессинге и презентации антигенных пептидов.В отличие от клеток Купфера, однако, мультивезикулярные компартменты, наблюдаемые в LSEC, не богаты MHC класса II, что может указывать на то, что LSEC не участвуют в презентации антигена [79-81]. Тем не менее, Knolle и др. [82,83] продемонстрировали, что и клетки Купфера, и LSEC имеют класс II MHC, и что обе эти клетки участвуют в презентации антигена. Однако LSEC не смогли вызвать дифференцировку в сторону воспалительного Th2 [82]. Более того, представление растворимых передающихся с кровью антигенов приводит в первую очередь к толерантности, а не к иммунному надзору.Известно, что LSEC экспрессируют CD80 и CD86, молекулы, которые присутствуют на профессиональных антигенпрезентирующих клетках, таких как дендритные клетки [14]. Кроме того, LSEC играют ключевую роль в опосредованном рецептором захвате, в деградации макромолекул из синусоидальной крови [84-86] и в удалении циркулирующих апоптотических телец [83,84]. Katz et al [18] сообщили о некоторых противоречивых данных, низком уровне или отсутствии MHC класса II, CD86 и CD11c. Однако они упомянули высокую способность поглощения AG in vivo и in vitro .Согласно Knolle et al [14,83], LSEC были неспособны стимулировать аллогенные Т-клетки.
LSEC, как известно, секретируют NO и могут вызывать апоптоз в различных типах раковых клеток, таких как лимфома и колоректальная карцинома [87,88]. Сообщалось также, что NO действует как цитолитический фактор при опосредованной макрофагами цитотоксичности раковых клеток [89].
Через семнадцать дней после инъекции клеток карциномы толстой кишки CC531s в брыжеечную вену наблюдаются метастазы в виде узелков диаметром 1-3 мм на поверхности долей печени.Когда синусоидальные клетки печени окрашивают in vivo с помощью FSA, не может быть обнаружено окрашивание в центре узелка метастаза (рисунок). На границе опухоли можно увидеть положительное окрашивание, но меньшей интенсивности, чем в нормальной ткани. Известно, что узелки диаметром 1-2 мм не имеют внутренней васкуляризации и что клетки получают питательные вещества и кислород просто путем диффузии (предваскулярная фаза) [90]. Формирование сосудов, однако, наблюдали с помощью конфокальной микроскопии в кластере клеток из 12 клеток CC531s через 24 часа после инъекции клеток CC531s (рисунок), и известно, что клетки карциномы толстой кишки продуцируют ангиогенные факторы, такие как VEGF [91].Однако даже несмотря на то, что ангиогенные факторы допускают образование сосудов в микрометастазах, как показано на рисунке, эти сосуды неспособны расширяться для обеспечения кровоснабжения в узелках макрометастазов, как показано на рисунке.
клеток CC531s вводили в брыжеечную вену и оставляли в кровотоке на 17 дней. За час до перфузионной фиксации в вену полового члена вводили FSA. FSA окрашивает только LSEC. Была проведена конфокальная микроскопия, и изображения были названы в честь соответствующих лазерных линий.A: Окрашивание FSA измеряли с помощью CLSM; флуоресценция наблюдалась только в части сканируемого поля; B: Просвечивающее изображение того же поля с областью опухоли в нижней части поля. Можно наблюдать образование крипт опухоли (Т); C: После объединения двух изображений внутри области опухоли не наблюдалось окрашивания. Размер изображения: 500 мкм × 500 мкм.
CC531 были помечены DiO, введенным в брыжеечную вену. Через 24 часа клетки Купфера (KC) окрашивали in vivo с помощью меченных TRITC латексных шариков и фиксировали печень перфузией.Была проведена конфокальная микроскопия, и изображения были названы в честь соответствующих лазерных линий. A: Визуализирована группа CC531; B: KC был визуализирован путем поглощения флуоресцентных латексных шариков; C: Остальная часть поля была исследована с функцией передачи; D: CC531s пролиферировал внутри паренхимы печени и внутри группы клеток CC531s был замечен сосуд. Сосуд намного прямее, чем нормальные синусоиды печени, что указывает на новообразованный сосуд. Размер изображения: 158,7 мкм × 158,7 мкм.
Структурные и функциональные аспекты печени и синусоидальных клеток печени в связи с метастазами карциномы толстой кишки
Печень является преобладающим местом рецидива заболевания после первоначальной терапевтической операции на толстой кишке, в основном из-за двух факторов.Во-первых, жизнеспособные опухолевые клетки могут выходить в портальный кровоток во время хирургических манипуляций и проникать в печень [41]. Во-вторых, серьезное хирургическое вмешательство вызывает временное послеоперационное ослабление иммунной системы [42–44]. Таким образом, временная иммуносупрессия, вызванная хирургическим вмешательством, связана с повышенным риском метастазирования. Когда рак толстой кишки распространяется на печень, удаление метастазов с помощью хирургической резекции, криотерапии или радиочастоты является единственным лечебным лечением [45]. Более того, подавляющее большинство пациентов не поддаются хирургической резекции из-за наличия множественных метастазов.Для разработки новых стратегий, направленных на предотвращение метастазирования, крайне важно понимать механизмы клеточной защиты от опухолевых клеток и механизмы ускользания от опухоли.
Цитотоксичность синусоидальных клеток по отношению к опухолевым клеткам
Когда опухолевые клетки проникают в сосудистое русло и метастазируют в печень, они сталкиваются с защитными механизмами, специфичными для печени. Клетки Купфера и NK-клетки печени являются основными резидентными клетками иммунного надзора, но синусоидальные эндотелиальные клетки также участвуют в этом процессе.
Клетки Купфера Самая важная функция клеток Купфера – защита от инфекций и опухолевых клеток. Клетки Купфера действуют как антигенпрезентирующие клетки и как эффекторные клетки, которые действуют непосредственно путем фагоцитоза или косвенно путем активации других клеток, например NK-клетки [46,47]. Хотя клетки Купфера постоянно действуют как мусорщики, они могут активироваться разными путями. Во-первых, их активацию могут запускать растворимые медиаторы. IFN-γ – это типичный фактор активации макрофагов.Он играет центральную роль в развитии иммунных ответов с преобладанием Th2 и влияет не только на макрофаги аутокринным образом, но и на другие иммунные клетки.
Одним из ключевых событий во время реакций врожденного иммунитета является продукция IL-12, в основном макрофагами [48]. IL-12 побуждает NK-клетки быстро секретировать IFN-γ, который, в свою очередь, активирует макрофаги на ранней стадии иммунного ответа. Он также индуцирует продукцию IFN-γ Т-клетками. IL-18, который продуцируется клетками Купфера и другими типами клеток, также участвует в усилении продукции IFN-γ Т-клетками [49,50].Макрофаги также секретируют IFN-γ при одновременной стимуляции IL-12 и IL-18. Известно, что IFN-γ является возможным редуктором метастазирования рака толстой кишки в печень [51].
Макрофаги также могут быть активированы путем прямого взаимодействия с микроорганизмами или бактериальными продуктами, такими как липополисахарид, глюкан, мурамилдипептид и липид A [52]. Ключевая роль IFN-γ в клиренсе различных внутриклеточных патогенов была подробно продемонстрирована [53,54]. Было описано, что макрофаги выделяют цитотоксический радикал NO [55,56]. Исследования in vitro показали, что NO вызывает митохондриальную дисфункцию в опухолевых клетках, за которой следует дисфункция мембранного барьера в синусоиде печени [57,58]. Другим важным цитотоксическим фактором, высвобождаемым активированными макрофагами, является фактор некроза опухоли альфа (TNF-α), который продуцируется как в растворимой, так и в мембраносвязанной формах. После связывания с его рецептором в клетке-мишени может быть индуцирован апоптоз [59].
Цитотоксичность макрофагов можно разделить на антителозависимую и антителозависимую цитотоксичность, опосредованную клетками.Оба пути зависят от контакта и вызывают гибель опухолевых клеток через несколько часов. Антителозависимая клеточно-опосредованная цитотоксичность основана на распознавании покрытой антителом мишени рецепторами Fc на эффекторных клетках [60-62]. При перекрестном связывании рецептора Fc происходит секреция цитотоксических медиаторов. Вероятно, участвует секреция активных форм кислорода, IL-1 и TNF-α [63]. Антител-независимая клеточно-опосредованная цитотоксичность включает связывание с макрофагом с последующей транслокацией лизосомных органелл к мишени [47].Более того, цитотоксичность по отношению к опухолевым мишеням включает цитолиз и фагоцитоз [64].
При определенных патофизиологических состояниях апоптоз носит хаотический и неизбирательный характер, может быть массивным и постоянно протекать в течение длительного периода времени [65]. Большое количество продуцируемых апоптотических телец фагоцитируется клетками Купфера. Недавно сообщалось, что поглощение апоптотических тел приводит к генерации лигандов смерти, таких как FasL и TNF-α на мембране клеток Купфера, но поглощение латексных шариков не вызывает подобного ответа [59].Это означает, что поглощение апоптотических тел вызывает дополнительный иммунологический ответ, включающий воспаление и фиброз печени [59,66].
Печеночные NK-клетки Цитотоксические лимфоциты (CTL) и NK-клетки вызывают гибель клеток-мишеней посредством гранул и путей, опосредованных рецепторами смерти. Апоптоз относится к организованной гибели клеток, которая необходима для поддержания гомеостаза. Характеристики апоптоза: конденсация хроматина, фрагментация ядер, образование пузырей на мембранах, сжатие клеток, деградация белка и фрагментация межнуклеосомной ДНК.Большинство морфологических изменений вызвано набором цистеиновых протеаз, которые активируются специфически в апоптотических клетках. Эти протеазы смерти гомологичны друг другу и являются членами большого семейства белков, известных как каспазы [67]. У людей было идентифицировано более десятка каспаз, и было высказано предположение, что около двух третей из них действуют при апоптозе [68,69]. Различные пути могут вызывать апоптоз, из которых наиболее известен путь Fas / FasL. Этот путь часто используется цитотоксическими Т-клетками и другими иммунокомпетентными клетками.Стимуляция рецептора Fas (CD95) лигандом Fas рекрутирует проформу инициатора каспазы 8 за счет взаимодействия с адаптерной молекулой Fas-ассоциированного домена смерти через домены смерти и эффекторные домены смерти. Это приводит к образованию комплекса, называемого сигнальным комплексом, вызывающим смерть. Затем прокаспаза 8 автокаталитически расщепляется с образованием активной инициаторной каспазы 8. Последствия активации каспазы 8 зависят от типа клетки. В клетках типа 1 другие члены семейства каспаз (например, каспаза 3) активируются напрямую [70].В клетках типа 2 активация каспазы 8 приводит к расщеплению проапоптотического члена семейства Bcl-2 Bid. Впоследствии Bid и Bax перемещаются в митохондрии, вызывая высвобождение цитохрома c . Это приводит к активации каспазы 9 за счет взаимодействия с адаптерной молекулой, активирующей апоптотический фактор протеазы. Каспаза 9 активирует каспазу 3, которая затем может выполнять свою функцию [71,72].
Гранулы CTL содержат различные белки, некоторые из которых, как известно, участвуют в гибели клеток-мишеней, такие как перфорин и гранзим.Описаны различные изоформы гранзимов. После того, как гранзим B попадает в клетку-мишень, он может непосредственно расщеплять прокаспазу 3, Bid и ингибитор каспазо-активируемой ДНКазы, тем самым вызывая апоптоз [71,73-75]. Смерть, вызванная гранзимом A, по-видимому, не зависит от путей, используемых гранзимом B [75,76]. Гранзим А не активирует каспазы в клетках-мишенях и не индуцирует расщепление других субстратов гранзима В. Функции других изоформ гранзима остаются неясными [76]. Перфорин образует трансмембранные поры и является важным активатором гранзим-опосредованного апоптоза [77].
Синусоидальные эндотелиальные клетки печени LSEC, как и клетки Купфера, экспрессируют рецептор Fc, который может участвовать в иммунологической защите. Было показано, что опосредованное FcR поглощение IgG-иммунного комплекса усиливает презентацию антигенов MHC класса II [78]. Этот процесс может происходить в компартменте, напоминающем мультивезикулярные компартменты, наблюдаемые в LSEC. Следовательно, возможно, что эти органеллы участвуют в процессинге и презентации антигенных пептидов.В отличие от клеток Купфера, однако, мультивезикулярные компартменты, наблюдаемые в LSEC, не богаты MHC класса II, что может указывать на то, что LSEC не участвуют в презентации антигена [79-81]. Тем не менее, Knolle и др. [82,83] продемонстрировали, что и клетки Купфера, и LSEC имеют класс II MHC, и что обе эти клетки участвуют в презентации антигена. Однако LSEC не смогли вызвать дифференцировку в сторону воспалительного Th2 [82]. Более того, представление растворимых передающихся с кровью антигенов приводит в первую очередь к толерантности, а не к иммунному надзору.Известно, что LSEC экспрессируют CD80 и CD86, молекулы, которые присутствуют на профессиональных антигенпрезентирующих клетках, таких как дендритные клетки [14]. Кроме того, LSEC играют ключевую роль в опосредованном рецептором захвате, в деградации макромолекул из синусоидальной крови [84-86] и в удалении циркулирующих апоптотических телец [83,84]. Katz et al [18] сообщили о некоторых противоречивых данных, низком уровне или отсутствии MHC класса II, CD86 и CD11c. Однако они упомянули высокую способность поглощения AG in vivo и in vitro .Согласно Knolle et al [14,83], LSEC были неспособны стимулировать аллогенные Т-клетки.
LSEC, как известно, секретируют NO и могут вызывать апоптоз в различных типах раковых клеток, таких как лимфома и колоректальная карцинома [87,88]. Сообщалось также, что NO действует как цитолитический фактор при опосредованной макрофагами цитотоксичности раковых клеток [89].
Через семнадцать дней после инъекции клеток карциномы толстой кишки CC531s в брыжеечную вену наблюдаются метастазы в виде узелков диаметром 1-3 мм на поверхности долей печени.Когда синусоидальные клетки печени окрашивают in vivo с помощью FSA, не может быть обнаружено окрашивание в центре узелка метастаза (рисунок). На границе опухоли можно увидеть положительное окрашивание, но меньшей интенсивности, чем в нормальной ткани. Известно, что узелки диаметром 1-2 мм не имеют внутренней васкуляризации и что клетки получают питательные вещества и кислород просто путем диффузии (предваскулярная фаза) [90]. Формирование сосудов, однако, наблюдали с помощью конфокальной микроскопии в кластере клеток из 12 клеток CC531s через 24 часа после инъекции клеток CC531s (рисунок), и известно, что клетки карциномы толстой кишки продуцируют ангиогенные факторы, такие как VEGF [91].Однако даже несмотря на то, что ангиогенные факторы допускают образование сосудов в микрометастазах, как показано на рисунке, эти сосуды неспособны расширяться для обеспечения кровоснабжения в узелках макрометастазов, как показано на рисунке.
клеток CC531s вводили в брыжеечную вену и оставляли в кровотоке на 17 дней. За час до перфузионной фиксации в вену полового члена вводили FSA. FSA окрашивает только LSEC. Была проведена конфокальная микроскопия, и изображения были названы в честь соответствующих лазерных линий.A: Окрашивание FSA измеряли с помощью CLSM; флуоресценция наблюдалась только в части сканируемого поля; B: Просвечивающее изображение того же поля с областью опухоли в нижней части поля. Можно наблюдать образование крипт опухоли (Т); C: После объединения двух изображений внутри области опухоли не наблюдалось окрашивания. Размер изображения: 500 мкм × 500 мкм.
CC531 были помечены DiO, введенным в брыжеечную вену. Через 24 часа клетки Купфера (KC) окрашивали in vivo с помощью меченных TRITC латексных шариков и фиксировали печень перфузией.Была проведена конфокальная микроскопия, и изображения были названы в честь соответствующих лазерных линий. A: Визуализирована группа CC531; B: KC был визуализирован путем поглощения флуоресцентных латексных шариков; C: Остальная часть поля была исследована с функцией передачи; D: CC531s пролиферировал внутри паренхимы печени и внутри группы клеток CC531s был замечен сосуд. Сосуд намного прямее, чем нормальные синусоиды печени, что указывает на новообразованный сосуд. Размер изображения: 158,7 мкм × 158,7 мкм.
Структурные и функциональные аспекты печени и синусоидальных клеток печени в связи с метастазами карциномы толстой кишки
Печень является преобладающим местом рецидива заболевания после первоначальной терапевтической операции на толстой кишке, в основном из-за двух факторов.Во-первых, жизнеспособные опухолевые клетки могут выходить в портальный кровоток во время хирургических манипуляций и проникать в печень [41]. Во-вторых, серьезное хирургическое вмешательство вызывает временное послеоперационное ослабление иммунной системы [42–44]. Таким образом, временная иммуносупрессия, вызванная хирургическим вмешательством, связана с повышенным риском метастазирования. Когда рак толстой кишки распространяется на печень, удаление метастазов с помощью хирургической резекции, криотерапии или радиочастоты является единственным лечебным лечением [45]. Более того, подавляющее большинство пациентов не поддаются хирургической резекции из-за наличия множественных метастазов.Для разработки новых стратегий, направленных на предотвращение метастазирования, крайне важно понимать механизмы клеточной защиты от опухолевых клеток и механизмы ускользания от опухоли.
Цитотоксичность синусоидальных клеток по отношению к опухолевым клеткам
Когда опухолевые клетки проникают в сосудистое русло и метастазируют в печень, они сталкиваются с защитными механизмами, специфичными для печени. Клетки Купфера и NK-клетки печени являются основными резидентными клетками иммунного надзора, но синусоидальные эндотелиальные клетки также участвуют в этом процессе.
Клетки Купфера Самая важная функция клеток Купфера – защита от инфекций и опухолевых клеток. Клетки Купфера действуют как антигенпрезентирующие клетки и как эффекторные клетки, которые действуют непосредственно путем фагоцитоза или косвенно путем активации других клеток, например NK-клетки [46,47]. Хотя клетки Купфера постоянно действуют как мусорщики, они могут активироваться разными путями. Во-первых, их активацию могут запускать растворимые медиаторы. IFN-γ – это типичный фактор активации макрофагов.Он играет центральную роль в развитии иммунных ответов с преобладанием Th2 и влияет не только на макрофаги аутокринным образом, но и на другие иммунные клетки.
Одним из ключевых событий во время реакций врожденного иммунитета является продукция IL-12, в основном макрофагами [48]. IL-12 побуждает NK-клетки быстро секретировать IFN-γ, который, в свою очередь, активирует макрофаги на ранней стадии иммунного ответа. Он также индуцирует продукцию IFN-γ Т-клетками. IL-18, который продуцируется клетками Купфера и другими типами клеток, также участвует в усилении продукции IFN-γ Т-клетками [49,50].Макрофаги также секретируют IFN-γ при одновременной стимуляции IL-12 и IL-18. Известно, что IFN-γ является возможным редуктором метастазирования рака толстой кишки в печень [51].
Макрофаги также могут быть активированы путем прямого взаимодействия с микроорганизмами или бактериальными продуктами, такими как липополисахарид, глюкан, мурамилдипептид и липид A [52]. Ключевая роль IFN-γ в клиренсе различных внутриклеточных патогенов была подробно продемонстрирована [53,54]. Было описано, что макрофаги выделяют цитотоксический радикал NO [55,56]. Исследования in vitro показали, что NO вызывает митохондриальную дисфункцию в опухолевых клетках, за которой следует дисфункция мембранного барьера в синусоиде печени [57,58]. Другим важным цитотоксическим фактором, высвобождаемым активированными макрофагами, является фактор некроза опухоли альфа (TNF-α), который продуцируется как в растворимой, так и в мембраносвязанной формах. После связывания с его рецептором в клетке-мишени может быть индуцирован апоптоз [59].
Цитотоксичность макрофагов можно разделить на антителозависимую и антителозависимую цитотоксичность, опосредованную клетками.Оба пути зависят от контакта и вызывают гибель опухолевых клеток через несколько часов. Антителозависимая клеточно-опосредованная цитотоксичность основана на распознавании покрытой антителом мишени рецепторами Fc на эффекторных клетках [60-62]. При перекрестном связывании рецептора Fc происходит секреция цитотоксических медиаторов. Вероятно, участвует секреция активных форм кислорода, IL-1 и TNF-α [63]. Антител-независимая клеточно-опосредованная цитотоксичность включает связывание с макрофагом с последующей транслокацией лизосомных органелл к мишени [47].Более того, цитотоксичность по отношению к опухолевым мишеням включает цитолиз и фагоцитоз [64].
При определенных патофизиологических состояниях апоптоз носит хаотический и неизбирательный характер, может быть массивным и постоянно протекать в течение длительного периода времени [65]. Большое количество продуцируемых апоптотических телец фагоцитируется клетками Купфера. Недавно сообщалось, что поглощение апоптотических тел приводит к генерации лигандов смерти, таких как FasL и TNF-α на мембране клеток Купфера, но поглощение латексных шариков не вызывает подобного ответа [59].Это означает, что поглощение апоптотических тел вызывает дополнительный иммунологический ответ, включающий воспаление и фиброз печени [59,66].
Печеночные NK-клетки Цитотоксические лимфоциты (CTL) и NK-клетки вызывают гибель клеток-мишеней посредством гранул и путей, опосредованных рецепторами смерти. Апоптоз относится к организованной гибели клеток, которая необходима для поддержания гомеостаза. Характеристики апоптоза: конденсация хроматина, фрагментация ядер, образование пузырей на мембранах, сжатие клеток, деградация белка и фрагментация межнуклеосомной ДНК.Большинство морфологических изменений вызвано набором цистеиновых протеаз, которые активируются специфически в апоптотических клетках. Эти протеазы смерти гомологичны друг другу и являются членами большого семейства белков, известных как каспазы [67]. У людей было идентифицировано более десятка каспаз, и было высказано предположение, что около двух третей из них действуют при апоптозе [68,69]. Различные пути могут вызывать апоптоз, из которых наиболее известен путь Fas / FasL. Этот путь часто используется цитотоксическими Т-клетками и другими иммунокомпетентными клетками.Стимуляция рецептора Fas (CD95) лигандом Fas рекрутирует проформу инициатора каспазы 8 за счет взаимодействия с адаптерной молекулой Fas-ассоциированного домена смерти через домены смерти и эффекторные домены смерти. Это приводит к образованию комплекса, называемого сигнальным комплексом, вызывающим смерть. Затем прокаспаза 8 автокаталитически расщепляется с образованием активной инициаторной каспазы 8. Последствия активации каспазы 8 зависят от типа клетки. В клетках типа 1 другие члены семейства каспаз (например, каспаза 3) активируются напрямую [70].В клетках типа 2 активация каспазы 8 приводит к расщеплению проапоптотического члена семейства Bcl-2 Bid. Впоследствии Bid и Bax перемещаются в митохондрии, вызывая высвобождение цитохрома c . Это приводит к активации каспазы 9 за счет взаимодействия с адаптерной молекулой, активирующей апоптотический фактор протеазы. Каспаза 9 активирует каспазу 3, которая затем может выполнять свою функцию [71,72].
Гранулы CTL содержат различные белки, некоторые из которых, как известно, участвуют в гибели клеток-мишеней, такие как перфорин и гранзим.Описаны различные изоформы гранзимов. После того, как гранзим B попадает в клетку-мишень, он может непосредственно расщеплять прокаспазу 3, Bid и ингибитор каспазо-активируемой ДНКазы, тем самым вызывая апоптоз [71,73-75]. Смерть, вызванная гранзимом A, по-видимому, не зависит от путей, используемых гранзимом B [75,76]. Гранзим А не активирует каспазы в клетках-мишенях и не индуцирует расщепление других субстратов гранзима В. Функции других изоформ гранзима остаются неясными [76]. Перфорин образует трансмембранные поры и является важным активатором гранзим-опосредованного апоптоза [77].
Синусоидальные эндотелиальные клетки печени LSEC, как и клетки Купфера, экспрессируют рецептор Fc, который может участвовать в иммунологической защите. Было показано, что опосредованное FcR поглощение IgG-иммунного комплекса усиливает презентацию антигенов MHC класса II [78]. Этот процесс может происходить в компартменте, напоминающем мультивезикулярные компартменты, наблюдаемые в LSEC. Следовательно, возможно, что эти органеллы участвуют в процессинге и презентации антигенных пептидов.В отличие от клеток Купфера, однако, мультивезикулярные компартменты, наблюдаемые в LSEC, не богаты MHC класса II, что может указывать на то, что LSEC не участвуют в презентации антигена [79-81]. Тем не менее, Knolle и др. [82,83] продемонстрировали, что и клетки Купфера, и LSEC имеют класс II MHC, и что обе эти клетки участвуют в презентации антигена. Однако LSEC не смогли вызвать дифференцировку в сторону воспалительного Th2 [82]. Более того, представление растворимых передающихся с кровью антигенов приводит в первую очередь к толерантности, а не к иммунному надзору.Известно, что LSEC экспрессируют CD80 и CD86, молекулы, которые присутствуют на профессиональных антигенпрезентирующих клетках, таких как дендритные клетки [14]. Кроме того, LSEC играют ключевую роль в опосредованном рецептором захвате, в деградации макромолекул из синусоидальной крови [84-86] и в удалении циркулирующих апоптотических телец [83,84]. Katz et al [18] сообщили о некоторых противоречивых данных, низком уровне или отсутствии MHC класса II, CD86 и CD11c. Однако они упомянули высокую способность поглощения AG in vivo и in vitro .Согласно Knolle et al [14,83], LSEC были неспособны стимулировать аллогенные Т-клетки.
LSEC, как известно, секретируют NO и могут вызывать апоптоз в различных типах раковых клеток, таких как лимфома и колоректальная карцинома [87,88]. Сообщалось также, что NO действует как цитолитический фактор при опосредованной макрофагами цитотоксичности раковых клеток [89].
Через семнадцать дней после инъекции клеток карциномы толстой кишки CC531s в брыжеечную вену наблюдаются метастазы в виде узелков диаметром 1-3 мм на поверхности долей печени.Когда синусоидальные клетки печени окрашивают in vivo с помощью FSA, не может быть обнаружено окрашивание в центре узелка метастаза (рисунок). На границе опухоли можно увидеть положительное окрашивание, но меньшей интенсивности, чем в нормальной ткани. Известно, что узелки диаметром 1-2 мм не имеют внутренней васкуляризации и что клетки получают питательные вещества и кислород просто путем диффузии (предваскулярная фаза) [90]. Формирование сосудов, однако, наблюдали с помощью конфокальной микроскопии в кластере клеток из 12 клеток CC531s через 24 часа после инъекции клеток CC531s (рисунок), и известно, что клетки карциномы толстой кишки продуцируют ангиогенные факторы, такие как VEGF [91].Однако даже несмотря на то, что ангиогенные факторы допускают образование сосудов в микрометастазах, как показано на рисунке, эти сосуды неспособны расширяться для обеспечения кровоснабжения в узелках макрометастазов, как показано на рисунке.
клеток CC531s вводили в брыжеечную вену и оставляли в кровотоке на 17 дней. За час до перфузионной фиксации в вену полового члена вводили FSA. FSA окрашивает только LSEC. Была проведена конфокальная микроскопия, и изображения были названы в честь соответствующих лазерных линий.A: Окрашивание FSA измеряли с помощью CLSM; флуоресценция наблюдалась только в части сканируемого поля; B: Просвечивающее изображение того же поля с областью опухоли в нижней части поля. Можно наблюдать образование крипт опухоли (Т); C: После объединения двух изображений внутри области опухоли не наблюдалось окрашивания. Размер изображения: 500 мкм × 500 мкм.
CC531 были помечены DiO, введенным в брыжеечную вену. Через 24 часа клетки Купфера (KC) окрашивали in vivo с помощью меченных TRITC латексных шариков и фиксировали печень перфузией.Была проведена конфокальная микроскопия, и изображения были названы в честь соответствующих лазерных линий. A: Визуализирована группа CC531; B: KC был визуализирован путем поглощения флуоресцентных латексных шариков; C: Остальная часть поля была исследована с функцией передачи; D: CC531s пролиферировал внутри паренхимы печени и внутри группы клеток CC531s был замечен сосуд. Сосуд намного прямее, чем нормальные синусоиды печени, что указывает на новообразованный сосуд. Размер изображения: 158,7 мкм × 158,7 мкм.
Структурные и функциональные аспекты печени и синусоидальных клеток печени в связи с метастазами карциномы толстой кишки
Печень является преобладающим местом рецидива заболевания после первоначальной терапевтической операции на толстой кишке, в основном из-за двух факторов.Во-первых, жизнеспособные опухолевые клетки могут выходить в портальный кровоток во время хирургических манипуляций и проникать в печень [41]. Во-вторых, серьезное хирургическое вмешательство вызывает временное послеоперационное ослабление иммунной системы [42–44]. Таким образом, временная иммуносупрессия, вызванная хирургическим вмешательством, связана с повышенным риском метастазирования. Когда рак толстой кишки распространяется на печень, удаление метастазов с помощью хирургической резекции, криотерапии или радиочастоты является единственным лечебным лечением [45]. Более того, подавляющее большинство пациентов не поддаются хирургической резекции из-за наличия множественных метастазов.Для разработки новых стратегий, направленных на предотвращение метастазирования, крайне важно понимать механизмы клеточной защиты от опухолевых клеток и механизмы ускользания от опухоли.
Цитотоксичность синусоидальных клеток по отношению к опухолевым клеткам
Когда опухолевые клетки проникают в сосудистое русло и метастазируют в печень, они сталкиваются с защитными механизмами, специфичными для печени. Клетки Купфера и NK-клетки печени являются основными резидентными клетками иммунного надзора, но синусоидальные эндотелиальные клетки также участвуют в этом процессе.
Клетки Купфера Самая важная функция клеток Купфера – защита от инфекций и опухолевых клеток. Клетки Купфера действуют как антигенпрезентирующие клетки и как эффекторные клетки, которые действуют непосредственно путем фагоцитоза или косвенно путем активации других клеток, например NK-клетки [46,47]. Хотя клетки Купфера постоянно действуют как мусорщики, они могут активироваться разными путями. Во-первых, их активацию могут запускать растворимые медиаторы. IFN-γ – это типичный фактор активации макрофагов.Он играет центральную роль в развитии иммунных ответов с преобладанием Th2 и влияет не только на макрофаги аутокринным образом, но и на другие иммунные клетки.
Одним из ключевых событий во время реакций врожденного иммунитета является продукция IL-12, в основном макрофагами [48]. IL-12 побуждает NK-клетки быстро секретировать IFN-γ, который, в свою очередь, активирует макрофаги на ранней стадии иммунного ответа. Он также индуцирует продукцию IFN-γ Т-клетками. IL-18, который продуцируется клетками Купфера и другими типами клеток, также участвует в усилении продукции IFN-γ Т-клетками [49,50].Макрофаги также секретируют IFN-γ при одновременной стимуляции IL-12 и IL-18. Известно, что IFN-γ является возможным редуктором метастазирования рака толстой кишки в печень [51].
Макрофаги также могут быть активированы путем прямого взаимодействия с микроорганизмами или бактериальными продуктами, такими как липополисахарид, глюкан, мурамилдипептид и липид A [52]. Ключевая роль IFN-γ в клиренсе различных внутриклеточных патогенов была подробно продемонстрирована [53,54]. Было описано, что макрофаги выделяют цитотоксический радикал NO [55,56]. Исследования in vitro показали, что NO вызывает митохондриальную дисфункцию в опухолевых клетках, за которой следует дисфункция мембранного барьера в синусоиде печени [57,58]. Другим важным цитотоксическим фактором, высвобождаемым активированными макрофагами, является фактор некроза опухоли альфа (TNF-α), который продуцируется как в растворимой, так и в мембраносвязанной формах. После связывания с его рецептором в клетке-мишени может быть индуцирован апоптоз [59].
Цитотоксичность макрофагов можно разделить на антителозависимую и антителозависимую цитотоксичность, опосредованную клетками.Оба пути зависят от контакта и вызывают гибель опухолевых клеток через несколько часов. Антителозависимая клеточно-опосредованная цитотоксичность основана на распознавании покрытой антителом мишени рецепторами Fc на эффекторных клетках [60-62]. При перекрестном связывании рецептора Fc происходит секреция цитотоксических медиаторов. Вероятно, участвует секреция активных форм кислорода, IL-1 и TNF-α [63]. Антител-независимая клеточно-опосредованная цитотоксичность включает связывание с макрофагом с последующей транслокацией лизосомных органелл к мишени [47].Более того, цитотоксичность по отношению к опухолевым мишеням включает цитолиз и фагоцитоз [64].
При определенных патофизиологических состояниях апоптоз носит хаотический и неизбирательный характер, может быть массивным и постоянно протекать в течение длительного периода времени [65]. Большое количество продуцируемых апоптотических телец фагоцитируется клетками Купфера. Недавно сообщалось, что поглощение апоптотических тел приводит к генерации лигандов смерти, таких как FasL и TNF-α на мембране клеток Купфера, но поглощение латексных шариков не вызывает подобного ответа [59].Это означает, что поглощение апоптотических тел вызывает дополнительный иммунологический ответ, включающий воспаление и фиброз печени [59,66].
Печеночные NK-клетки Цитотоксические лимфоциты (CTL) и NK-клетки вызывают гибель клеток-мишеней посредством гранул и путей, опосредованных рецепторами смерти. Апоптоз относится к организованной гибели клеток, которая необходима для поддержания гомеостаза. Характеристики апоптоза: конденсация хроматина, фрагментация ядер, образование пузырей на мембранах, сжатие клеток, деградация белка и фрагментация межнуклеосомной ДНК.Большинство морфологических изменений вызвано набором цистеиновых протеаз, которые активируются специфически в апоптотических клетках. Эти протеазы смерти гомологичны друг другу и являются членами большого семейства белков, известных как каспазы [67]. У людей было идентифицировано более десятка каспаз, и было высказано предположение, что около двух третей из них действуют при апоптозе [68,69]. Различные пути могут вызывать апоптоз, из которых наиболее известен путь Fas / FasL. Этот путь часто используется цитотоксическими Т-клетками и другими иммунокомпетентными клетками.Стимуляция рецептора Fas (CD95) лигандом Fas рекрутирует проформу инициатора каспазы 8 за счет взаимодействия с адаптерной молекулой Fas-ассоциированного домена смерти через домены смерти и эффекторные домены смерти. Это приводит к образованию комплекса, называемого сигнальным комплексом, вызывающим смерть. Затем прокаспаза 8 автокаталитически расщепляется с образованием активной инициаторной каспазы 8. Последствия активации каспазы 8 зависят от типа клетки. В клетках типа 1 другие члены семейства каспаз (например, каспаза 3) активируются напрямую [70].В клетках типа 2 активация каспазы 8 приводит к расщеплению проапоптотического члена семейства Bcl-2 Bid. Впоследствии Bid и Bax перемещаются в митохондрии, вызывая высвобождение цитохрома c . Это приводит к активации каспазы 9 за счет взаимодействия с адаптерной молекулой, активирующей апоптотический фактор протеазы. Каспаза 9 активирует каспазу 3, которая затем может выполнять свою функцию [71,72].
Гранулы CTL содержат различные белки, некоторые из которых, как известно, участвуют в гибели клеток-мишеней, такие как перфорин и гранзим.Описаны различные изоформы гранзимов. После того, как гранзим B попадает в клетку-мишень, он может непосредственно расщеплять прокаспазу 3, Bid и ингибитор каспазо-активируемой ДНКазы, тем самым вызывая апоптоз [71,73-75]. Смерть, вызванная гранзимом A, по-видимому, не зависит от путей, используемых гранзимом B [75,76]. Гранзим А не активирует каспазы в клетках-мишенях и не индуцирует расщепление других субстратов гранзима В. Функции других изоформ гранзима остаются неясными [76]. Перфорин образует трансмембранные поры и является важным активатором гранзим-опосредованного апоптоза [77].
Синусоидальные эндотелиальные клетки печени LSEC, как и клетки Купфера, экспрессируют рецептор Fc, который может участвовать в иммунологической защите. Было показано, что опосредованное FcR поглощение IgG-иммунного комплекса усиливает презентацию антигенов MHC класса II [78]. Этот процесс может происходить в компартменте, напоминающем мультивезикулярные компартменты, наблюдаемые в LSEC. Следовательно, возможно, что эти органеллы участвуют в процессинге и презентации антигенных пептидов.В отличие от клеток Купфера, однако, мультивезикулярные компартменты, наблюдаемые в LSEC, не богаты MHC класса II, что может указывать на то, что LSEC не участвуют в презентации антигена [79-81]. Тем не менее, Knolle и др. [82,83] продемонстрировали, что и клетки Купфера, и LSEC имеют класс II MHC, и что обе эти клетки участвуют в презентации антигена. Однако LSEC не смогли вызвать дифференцировку в сторону воспалительного Th2 [82]. Более того, представление растворимых передающихся с кровью антигенов приводит в первую очередь к толерантности, а не к иммунному надзору.Известно, что LSEC экспрессируют CD80 и CD86, молекулы, которые присутствуют на профессиональных антигенпрезентирующих клетках, таких как дендритные клетки [14]. Кроме того, LSEC играют ключевую роль в опосредованном рецептором захвате, в деградации макромолекул из синусоидальной крови [84-86] и в удалении циркулирующих апоптотических телец [83,84]. Katz et al [18] сообщили о некоторых противоречивых данных, низком уровне или отсутствии MHC класса II, CD86 и CD11c. Однако они упомянули высокую способность поглощения AG in vivo и in vitro .Согласно Knolle et al [14,83], LSEC были неспособны стимулировать аллогенные Т-клетки.
LSEC, как известно, секретируют NO и могут вызывать апоптоз в различных типах раковых клеток, таких как лимфома и колоректальная карцинома [87,88]. Сообщалось также, что NO действует как цитолитический фактор при опосредованной макрофагами цитотоксичности раковых клеток [89].
Через семнадцать дней после инъекции клеток карциномы толстой кишки CC531s в брыжеечную вену наблюдаются метастазы в виде узелков диаметром 1-3 мм на поверхности долей печени.Когда синусоидальные клетки печени окрашивают in vivo с помощью FSA, не может быть обнаружено окрашивание в центре узелка метастаза (рисунок). На границе опухоли можно увидеть положительное окрашивание, но меньшей интенсивности, чем в нормальной ткани. Известно, что узелки диаметром 1-2 мм не имеют внутренней васкуляризации и что клетки получают питательные вещества и кислород просто путем диффузии (предваскулярная фаза) [90]. Формирование сосудов, однако, наблюдали с помощью конфокальной микроскопии в кластере клеток из 12 клеток CC531s через 24 часа после инъекции клеток CC531s (рисунок), и известно, что клетки карциномы толстой кишки продуцируют ангиогенные факторы, такие как VEGF [91].Однако даже несмотря на то, что ангиогенные факторы допускают образование сосудов в микрометастазах, как показано на рисунке, эти сосуды неспособны расширяться для обеспечения кровоснабжения в узелках макрометастазов, как показано на рисунке.
клеток CC531s вводили в брыжеечную вену и оставляли в кровотоке на 17 дней. За час до перфузионной фиксации в вену полового члена вводили FSA. FSA окрашивает только LSEC. Была проведена конфокальная микроскопия, и изображения были названы в честь соответствующих лазерных линий.A: Окрашивание FSA измеряли с помощью CLSM; флуоресценция наблюдалась только в части сканируемого поля; B: Просвечивающее изображение того же поля с областью опухоли в нижней части поля.


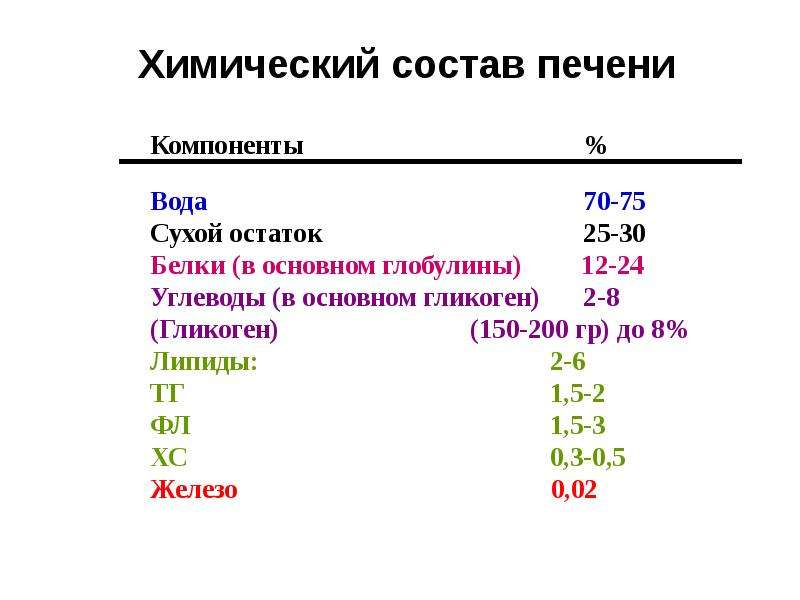 Недостаточное потребление витамина В6 сопровождается снижением аппетита, нарушением состояния кожных покровов, развитием гомоцистеинемии, анемии.
Недостаточное потребление витамина В6 сопровождается снижением аппетита, нарушением состояния кожных покровов, развитием гомоцистеинемии, анемии.


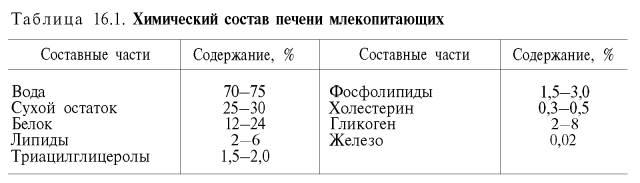
 Отличается приятным горьковатым вкусом и нежной консистенцией в приготовленном виде. Пользуется популярностью в кулинарии, благодаря значительной пищевой ценности. Употребляется в пищу преимущественно в отварном и тушеном, реже в жареном виде, а также используется при производстве различных мясных деликатесов.
Отличается приятным горьковатым вкусом и нежной консистенцией в приготовленном виде. Пользуется популярностью в кулинарии, благодаря значительной пищевой ценности. Употребляется в пищу преимущественно в отварном и тушеном, реже в жареном виде, а также используется при производстве различных мясных деликатесов. Благодаря этому, перечень блюд, которые готовятся из говяжьей печени, чрезвычайно широк. Данный субпродукт употребляют в пищу в отварном, жареном и тушеном виде, используя для приготовления салатов и закусок, супов-пюре и котлет, запеканок и паштетов, колбасных изделий и рулетов, бефстроганов, шашлыков, выпечных хлебобулочных изделий.
Благодаря этому, перечень блюд, которые готовятся из говяжьей печени, чрезвычайно широк. Данный субпродукт употребляют в пищу в отварном, жареном и тушеном виде, используя для приготовления салатов и закусок, супов-пюре и котлет, запеканок и паштетов, колбасных изделий и рулетов, бефстроганов, шашлыков, выпечных хлебобулочных изделий.
 Дело в том, что данный субпродукт в свежем виде отличается крайне непродолжительными сроками хранения: при комнатной температуре – около 12 часов, при температуре от 4 до 8 градусов – не более 2-3 суток. В замороженном виде говяжья печень хранится гораздо дольше – до нескольких месяцев при температуре не выше минус 16 градусов по Цельсию. При этом ее следует размораживать постепенно, избегая излишне агрессивного теплового воздействия.
Дело в том, что данный субпродукт в свежем виде отличается крайне непродолжительными сроками хранения: при комнатной температуре – около 12 часов, при температуре от 4 до 8 градусов – не более 2-3 суток. В замороженном виде говяжья печень хранится гораздо дольше – до нескольких месяцев при температуре не выше минус 16 градусов по Цельсию. При этом ее следует размораживать постепенно, избегая излишне агрессивного теплового воздействия.
 При скоплении билирубина кожа и глаза желтеют.
При скоплении билирубина кожа и глаза желтеют. Он отвечает за тысячи биохимических реакций.
Он отвечает за тысячи биохимических реакций.