строение, свойства, функции — урок.
 Биология, Общие биологические закономерности (9–11 класс).
Биология, Общие биологические закономерности (9–11 класс).Среди органических веществ клетки самыми разнообразными по свойствам и выполняемым функциям являются белки, или протеины. В белках, в отличии от углеводов и липидов, кроме углерода, кислорода и водорода содержится азот, а также могут присутствовать атомы серы, фосфора и железа.
Белки — это биополимеры, мономерами в которых служат аминокислоты. В образовании всего разнообразия белков участвует \(20\) α-аминокислот. Молекулы аминокислот имеют две функциональные группы: карбоксильную (кислотную) и аминогруппу (основную).
Рис. \(1\). Молекула аминокислоты
Аминогруппа и карбоксильная группа способны взаимодействовать между собой с отщеплением воды и образованием пептидной связи CO−NH. Пептидными связями молекулы аминокислот соединяются друг с другом в длинные цепи. Число остатков аминокислот в цепи может составлять несколько сотен и даже тысяч.
Структура белков
Порядок соединения аминокислот в макромолекуле белка называют первичной структурой. Для каждого типа белка эта структура уникальна. Она определяет структуры высших уровней, свойства белка и его функции.
Полипептидная цепь сворачивается в спираль за счёт образования водородных связей между группировками атомов −NH и −CO, расположенными на разных участках макромолекулы. Эту спираль называют вторичной структурой белка.
Третичная структура белка возникает при взаимодействии радикалов аминокислот, а также за счёт дисульфидных мостиков, водородных и ионных связей. Молекула белка принимает форму
У некоторых белков формируется четвертичная структура. Она представляет собой комплекс нескольких макромолекул, имеющих третичную структуру. Четвертичную структуру удерживают непрочные ионные и водородные связи, а также гидрофобные взаимодействия.
Четвертичную структуру удерживают непрочные ионные и водородные связи, а также гидрофобные взаимодействия.
Рис. \(2\). Структуры белка
Белки могут соединяться с углеводами, жирами и нуклеиновыми кислотами с образованием комплексных соединений: гликопротеинов, липопротеинов, нуклеопротеинов.
Под действием внешних факторов: облучения, нагревания, некоторых химических веществ и др. — происходит нарушение пространственной структуры белковых молекул. Этот процесс называется денатурацией.
Сначала происходит разрушение четвертичной структуры, потом третичной и вторичной. Первичная структура при денатурации сохраняется, но белок утрачивает свои свойства и функции.
Денатурация в некоторых случаях обратима. Обратный процесс называется ренатурацией.
Рис. \(3\). Денатурация и ренатурация белка
Разрушение первичной структуры необратимо. Оно происходит при гидролизе белка — макромолекулы распадаются на отдельные аминокислоты. Такой процесс идёт в органах пищеварения животных и в лизосомах клеток под действием гидролитических ферментов.
Оно происходит при гидролизе белка — макромолекулы распадаются на отдельные аминокислоты. Такой процесс идёт в органах пищеварения животных и в лизосомах клеток под действием гидролитических ферментов.
Функции белков
1. Важнейшей функцией белков является каталитическая, или ферментативная. Белки-ферменты участвуют во всех биохимических реакциях, протекающих в клетке, и повышают скорость этих реакций во много раз. Для каждой реакции существует особый фермент.
2. Белки выполняют структурную (строительную) функцию. Они входят в состав плазматических мембран, образуют соединительные ткани (эластин и коллаген), волосы и ногти (кератин).
Рис. \(4\). Структурные белки в плазматической мембране
3. Сигнальную функцию также осуществляют белки, встроенные в мембрану. Под действием внешних факторов эти белки изменяют третичную структуру, что отражается на функционировании клетки.
4. Транспортная функция белков проявляется в переносе ионов через клеточные мембраны, транспорте гемоглобином крови кислорода и углекислого газа, альбуминами плазмы — жирных кислот и т. д.
5. Двигательную функцию обеспечивают белки актин и миозин, способные сокращаться и растягиваться. Они приводят в движение реснички и жгутики одноклеточных организмов, сокращают мышцы у животных.
Рис. \(5\). Сократительные белки
6. Защитная функция обеспечивается антителами иммунной системы организма, белками системы свёртывании крови (фибриногеном, протомбином и др.).
7. Регуляторную функцию выполняют белки-гормоны (инсулин, тиреотропин, соматотропин, глюкагон и др.).
8. Энергетическую функцию белки выполняют после израсходования запасов углеводов и жиров. При полном расщеплении \(1\) г белка до конечных продуктов выделяется \(17,6\) кДж энергии.
Источники:
Рис. 1. Молекула аминокислоты. Автор: X-romix – собственная работа, Общественное достояние, https://commons.wikimedia.org/w/index.php?curid=10280776. 09.09.2021.
Рис. 2. Структуры белка. https://image.shutterstock.com/image-vector/protein-structure-primary-secondary-tertiary-600w-1474657079
Рис. 3. Денатурация и ренатурация белка. © ЯКласс.
Рис. 4. Структурные белки в плазматической мембран. https://shutterstock.puzzlepix.hu/kep/376416385е
Рис. 5. Сократительные белки. © ЯКласс.
1. Особенности химического состава клетки
Химические элементы клетки
Живые организмы состоят из веществ, образованных атомами тех же химических элементов, которые входят в состав тел неживой природы. Этот факт говорит о взаимосвязи живой и неживой природы. В клетках разных живых организмов находятся атомы одинаковых химических элементов, что подтверждает единство всех живых организмов.
Из известных в настоящее время более \(115\) элементов около \(80\) обнаружено в составе клетки.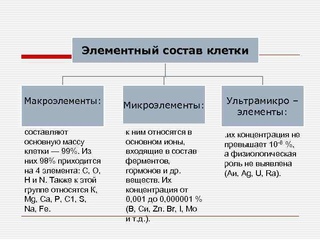
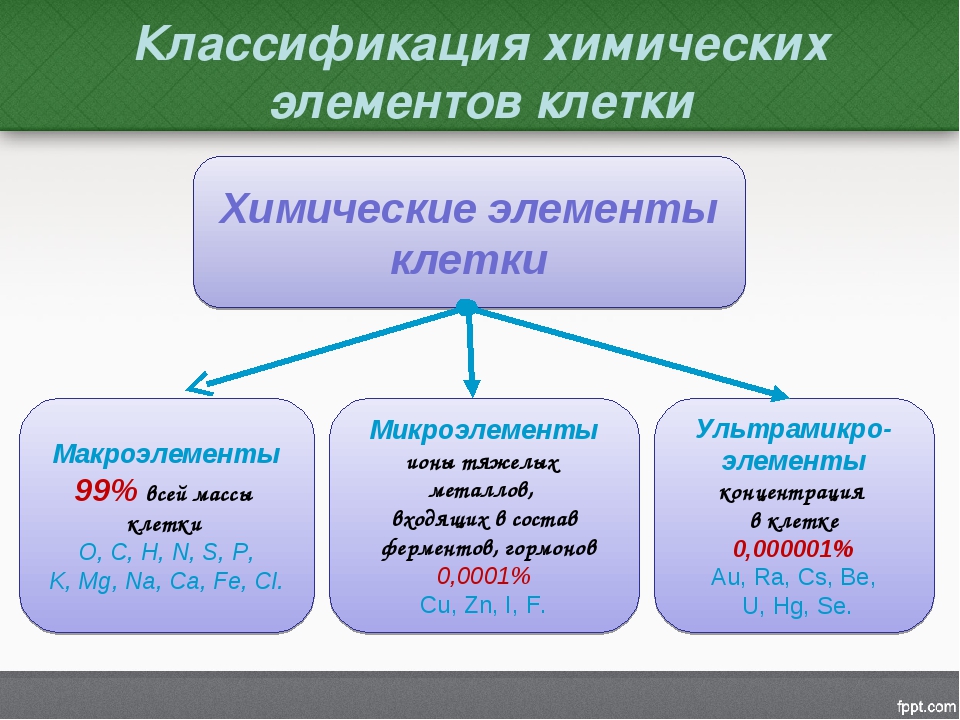
В зависимости от содержания химических элементов в клетках живых организмов их делят на три группы.
К макроэлементам относят элементы, содержание которых превышает \(0,001\) % от массы тела. \(98\) % массы любого организма составляют органогены: кислород, углерод, водород и азот.
- Кислород (до \(75\) %) входит в состав воды, органических и минеральных веществ клетки.
- Углерод (около \(15\) %) является обязательной составной частью всех органических молекул.
- Водород (\(8\) %) содержится в воде и в органических веществах.
- Азот (около \(3\) %) входит в состав белков, нуклеиновых кислот, АТФ.
Приблизительно \(2\) % от массы клетки приходится ещё на восемь макроэлементов. Это магний (Mg), натрий (Na), кальций (Ca), железо (Fe), калий (K), фосфор (P), хлор (Cl), сера (S).
К микроэлементам относятся те элементы, на долю которых приходится от \(0,000001\) % до \(0,001\) %: бор (B), никель (Ni), кобальт (Co), медь (Cu), молибден (Mo), цинк (Zn) и др.
Третья группа — ультрамикроэлементы, содержание которых не превышает \(0,000001\) %: уран (U), радий (Ra), золото (Au), ртуть (Hg), свинец (Pb), цезий (Cs), селен (Se) и др.
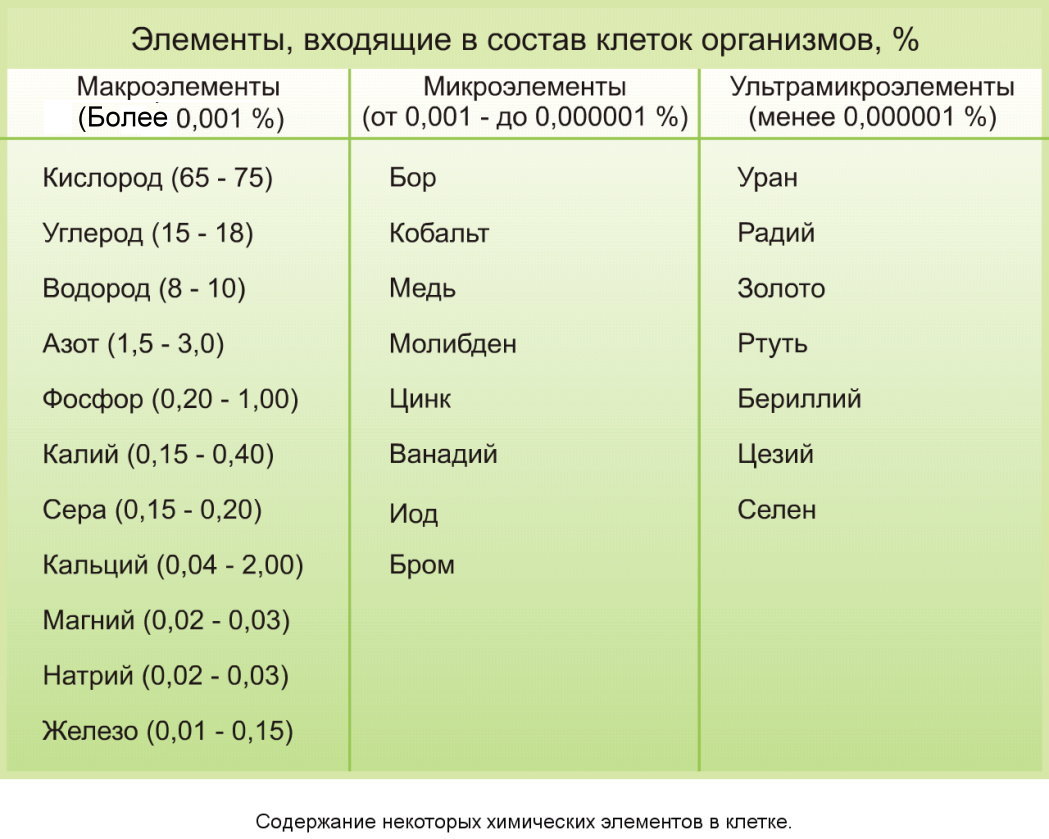
Рис. \(1\). Содержание химических элементов в живых организмах
Количество химического элемента не определяет его значение для организма. Например, йод относится к микроэлементам, но он входит в состав гормонов щитовидной железы, которые регулируют обмен веществ в организме человека.
Химические вещества клетки
Элементы в виде атомов образуют молекулы неорганических и органических соединений клетки.
Рис. \(2\). Содержание химических веществ в клетке
К неорганическим соединениям относятся вода и минеральные соли.
Органические соединения характерны только для живых организмов, в то время как неорганические существуют и в неживой природе. К органическим веществам относятся соединения углерода, содержащие также атомы водорода, кислорода, азота, фосфора.
К органическим веществам относятся соединения углерода, содержащие также атомы водорода, кислорода, азота, фосфора.
В клетках находятся низкомолекулярные соединения: аминокислоты, моносахариды, нуклеотиды, витамины, а также высокомолекулярные (полимеры): белки, полисахариды, нуклеиновые кислоты.
Рис. \(3\). Органические вещества клетки
Молекулы этих веществ (макромолекулы) состоят из большого числа повторяющихся звеньев. Белки, полисахариды и нуклеиновые кислоты содержатся во всех живых клетках и выполняют важнейшие функции, обеспечивающие жизнедеятельность клетки. Поэтому их называют биополимерами.
Простые вещества, из которых образуются макромолекулы, называются мономерами. Мономерами нуклеиновых кислот являются нуклеотиды, белков — аминокислоты, а макромолекулы полисахаридов состоят из остатков глюкозы.Рис. \(4\). Модель молекулы белка
Источники:
Рис. 1. Содержание химических элементов в живых организмах © ЯКласс.
1. Содержание химических элементов в живых организмах © ЯКласс.
Рис. 2. Содержание химических веществ в клетке © ЯКласс.
Рис. 3. Органические вещества клетки © ЯКласс.
Рис. 4. Модель молекулы белка https://cdn.pixabay.com/photo/2015/08/02/23/26/adrenomedullin-872350_960_720.jpg. 09.09.2021.
3. Минеральные вещества и их роль в клетке
Для нормальной жизнедеятельности организмов требуются минеральные соли. В клетке они находятся в твёрдом или в растворённом виде. Растворённые соли диссоциированы на ионы. Наиболее важными являются катионы металлов: калия K+, натрия Na+, кальция Ca2+, магния Mg2+, и анионы: Cl−, h3PO4−, HPO42−, HCO3−, CO32−.
Роль минеральных солей в клетке разная. Так, ионы калия и натрия обеспечивают возбудимость клеток. Внутри клетки больше ионов K+ , а снаружи всегда больше содержание Na+, что приводит к возникновению разности потенциалов на клеточной мембране, обеспечивает раздражимость клеток и передачу возбуждения по нервам или мышцам. Перенос ионов через мембрану клетки осуществляется натрий-калиевым насосом и происходит с затратами АТФ (активный транспорт).
Перенос ионов через мембрану клетки осуществляется натрий-калиевым насосом и происходит с затратами АТФ (активный транспорт).
Рис. \(1\). Натриево-калиевый насос
Ионы кальция участвуют в регуляции мышечных сокращений, необходимы для процесса свёртывания крови. Твёрдые соли кальция входят в состав костной ткани, содержатся в раковинах моллюсков и панцирях ракообразных.
Ионы магния входят в состав хлорофилла, а ионы железа — в состав гемоглобина.
Катионы многих металлов (магния, кальция, железа, меди, кобальта, цинка, марганца и др.) необходимы для синтеза некоторых ферментов, гормонов и витаминов.
Анионы фосфорной и угольной кислот образуют буферные системы, поддерживающие на постоянном уровне содержание ионов водорода в клетке (рН среды). Анионы HPO42− и h3PO4− (фосфатная буферная система) обеспечивают рН цитоплазмы клеток в пределах \(6,9\)–\(7,4\). Анионы HCO3− и CO32− (бикарбонатная буферная система) поддерживают значение рН плазмы крови \(7,4\).
Анионы HCO3− и CO32− (бикарбонатная буферная система) поддерживают значение рН плазмы крови \(7,4\).
Минеральные соли, содержащие азот и фосфор, нужны для образования белков, ДНК, РНК, АТФ и др.
Фосфаты входят в состав костной и зубной ткани. Хлорид-ионы необходимы для образования соляной кислоты, содержащейся в желудочном соке, а сульфат ионы — для синтеза некоторых аминокислот.
Недостаток минеральных солей приводит к нарушению процессов обмена веществ и негативно сказывается на жизнедеятельности клетки.
Источники:
Рис. 1. Натриево-калиевый насос © ЯКласс.
Химический состав клетки – это… Что такое Химический состав клетки?
Каждая клетка содержит множество химических элементов, участвующих в различных химических реакциях. Химические процессы, протекающие в клетке — одно из основных условий её жизни, развития и функционирования. Одних химических элементов в клетке больше, других — меньше.
На атомарном уровне различий между органическим и неорганическим миром живой природы нет: живые организмы состоят из тех же атомов, что и тела неживой природы. Однако соотношение разных химических элементов в живых организмах и в земной коре сильно различается. Кроме того, живые организмы могут отличаться от окружающей их среды по изотопному составу химических элементов.
Условно все элементы клетки можно разделить на три группы.
Макроэлементы
К макроэлементам относят кислород (65—75 %), углерод (15—18 %), водород (8—10 %), азот (2,0—3,0 %), калий (0,15—0,4 %), сера (0,15—0,2 %), фосфор (0,2—1,0 %), хлор (0,05—0,1 %), магний (0,02—0,03 %), натрий (0,02—0,03 %), кальций (0,04—2,00 %), железо (0,01—0,015 %). Такие элементы, как C, O, H, N, S, P входят в состав органических соединений.
Углерод — входит в состав всех органических веществ; скелет из атомов углерода составляет их основу. Кроме того, в виде CO2 фиксируется в процессе фотосинтеза и выделяется в ходе дыхания, в виде CO (в низких концентрациях) участвует в регуляции клеточных функций, в виде CaCO3 входит в состав минеральных скелетов.
Кислород — входит в состав практически всех органических веществ клетки. Образуется в ходе фотосинтеза при фотолизе воды. Для аэробных организмов служит окислителем в ходе клеточного дыхания, обеспечивая клетки энергией. В наибольших количествах в живых клетках содержится в составе воды.
Водород — входит в состав всех органических веществ клетки. В наибольших количествах содержится в составе воды. Некоторые бактерии окисляют молекулярный водород для получения энергии.
Азот — входит в состав белков, нуклеиновых кислот и их мономеров — аминокислот и нуклеотидов. Из организма животных выводится в составе аммиака, мочевины, гуанина или мочевой кислоты как конечный продукт азотного обмена. В виде оксида азота NO (в низких концентрациях) участвует в регуляции кровяного давления.
Сера — входит в состав серосодержащих аминокислот, поэтому содержится в большинстве белков. В небольших количествах присутствует в виде сульфат-иона в цитоплазме клеток и межклеточных жидкостях.
Фосфор — входит в состав АТФ, других нуклеотидов и нуклеиновых кислот (в виде остатков фосфорной кислоты), в состав костной ткани и зубной эмали (в виде минеральных солей), а также присутствует в цитоплазме и межклеточных жидкостях (в виде фосфат-ионов).
Магний — кофактор многих ферментов, участвующих в энергетическом обмене и синтезе ДНК; поддерживает целостность рибосом и митохондрий, входит в состав хлорофилла. В животных клетках необходим для функционирования мышечных и костных систем.
Кальций — участвует в свёртывании крови, а также служит одним из универсальных вторичных посредников, регулируя важнейшие внутриклеточные процессы (в том числе участвует в поддержании мембранного потенциала, необходим для мышечного сокращения и экзоцитоза). Нерастворимые соли кальция участвуют в формировании костей и зубов позвоночных и минеральных скелетов беспозвоночных.
Натрий — участвует в поддержании мембранного потенциала, генерации нервного импульса, процессах осморегуляции (в том числе в работе почек у человека) и создании буферной системы крови.
Калий — участвует в поддержании мембранного потенциала, генерации нервного импульса, регуляции сокращения сердечной мышцы.Содержится в межклеточных веществах.
Хлор — поддерживает электронейтральность клетки.
Микроэлементы
К микроэлементам, составляющим от 0,001 % до 0,000001 % массы тела живых существ, относят ванадий, германий, йод (входит в состав тироксина, гормона щитовидной железы), кобальт (витамин В12), марганец, никель, рутений, селен, фтор (зубная эмаль), медь, хром, цинк
Цинк — входит в состав ферментов, участвующих в спиртовом брожении, в состав инсулина
Медь — входит в состав окислительных ферментов, участвующих в синтезе цитохромов.
Селен – участвует в регуляторных процессах организма.
Ультрамикроэлементы
Ультрамикроэлементы составляют менее 0,0000001 % в организмах живых существ, к ним относят золото, серебро оказывают бактерицидное воздействие, ртуть подавляет обратное всасывание воды в почечных канальцах, оказывая воздействие на ферменты. Так же к ультрамикроэлементам относят платину и цезий. Некоторые к этой группе относят и селен, при его недостатке развиваются раковые заболевания. Функции ультрамикроэлементов еще мало понятны.
Так же к ультрамикроэлементам относят платину и цезий. Некоторые к этой группе относят и селен, при его недостатке развиваются раковые заболевания. Функции ультрамикроэлементов еще мало понятны.
Молекулярный состав клетки
| Соединения | |||
| Неорганические | Органические | ||
| Вода Минеральные соли | 70—80 % 1,0—1,5 % | Белки Углеводы Жиры Нуклеиновые кислоты АТФ, соли и др. вещества | 10—20 % 0,2—2,0 % 1—5 % 1,0—2,0 % 0,1—0,5 % |
См. также
«Химический состав клетки Макро- и микроэлементы» (10 класс) Задачи
Тема урока: «Химический состав клетки. Макро- и микроэлементы»
(10 класс)
Задачи: углубить знания о химическом составе
клетки: макро – и микроэлементах, их
роли в клетке; сформировать умение
доказывать материальное единство мира
на основе знаний об элементарном составе
клетки, используя проектную деятельность
развивать исследовательские способности
учащихся, воспитание культуры питания.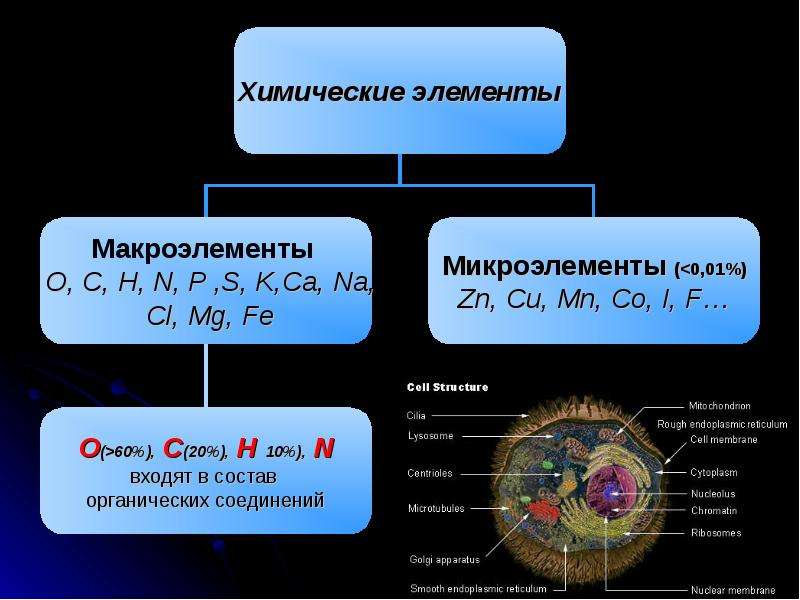
Оборудование: таблица, иллюстрирующая содержание химических элементов в клетке, презентации учащихся.
1.Орг. момент.
2.Ход урока.
1.Актуализация знаний. Курс общей биологии мы начинали с вами с изучения уровней организации живых организмов. Давайте с вами вспомним, какие уровни организации живой природы выделяют ученые? (ответ учащихся)
-На каком уровне начинается обмен веществ и превращение энергии?
Молекулярный уровень – это самый низкий уровень организации живого, представленный отдельными молекулами органических и неорганических веществ, входящих в состав клеток организма. Жизнедеятельность всех живых систем проявляется во взаимодействии молекул различных химических веществ.
– Назовите химические элементы, содержание которых в клетке преобладает?(Н, О,С,N)
–
Встречаются ли эти химические элементы
в неживой природе? О чем это свидетельствует?
(Живые тела состоят из тех же химических
элементов, что и неживые тела).
2.Изучение нового материала.
Сегодня на уроке мы с вами познакомимся с ролью основных химических элементов, входящих в состав клеток живых организмов.
В составе живой природы обнаружено более 80 химических элементов, но только роль 27 из них изучена.
Используя текст учебника, добавьте схему в своей тетради, изображенную на доске.
Химические элементы
Макроэлементы Ультрамикроэлементы
__________________%
_______________% Микроэлементы
_______________%__ Роль______________
Роль___________
Роль_____________
Каждый из химических элементов выполняет важную функцию в клетке.
– Приведите примеры о роли некоторых химических элементов из вашего личного опыта, из курса биологии, а так же из рекламных роликов, идущих на телевидении.
Запишите в своих тетрадях роль основных химических элементов ( самостоятельная работа учащихся с текстом учебника)
О, Н
– входят в состав воды.
С, О, Н, N – в составе белков, липидов, нуклеиновых кислот, полисахаридов.
К, Na, Cl – проведение нервного импульса.
Ca – компонент костей, зубов, необходим для мышечного сокращения, компонент свертывания крови.
Mg – структурный компонент хлорофилла, поддерживает работу рибосом и митохондрий.
Fe – структурный компонент гемоглобина, миоглобина.
S – в составе серосодержащих аминокислот.
P – в составе нуклеиновых кислот, костной ткани.
Mn, Zn, Cu – активаторы ферментов, влияют на процессы тканевого дыхания.
Zn – в составе инсулина.
Co – в составе витамина В12.
J – в составе тироксина.
F – в составе эмали зубов.
К
сегодняшнему уроку вы получили опережающее
задание составить меню с учетом нехватки
определенного химического элемента.
Давайте посмотрим, что у вас получилось (представление учащимися своих презентаций).
Закрепление. 1) Работа с дидактическими карточками (карточку можно дать индивидуально или организовать работу в парах).
Определите соответствие функции химическому элементу.
Ca – 1) в составе инсулина.
Mg – 2 структурный компонент хлорофилла, поддерживает
P – работу рибосом и митохондрий.
Fe – 3) в составе эмали зубов.
F – 4) в составе тироксина
J – 5) структурный компонент гемоглобина, миоглобина.
Zn–
6) в составе
серосодержащих аминокислот.
Co – 7) в составе витамина В12.
8) в составе нуклеиновых кислот, костной ткани.
9) компонент костей, зубов, необходим для мышечного
S – сокращения, компонент свертывания крови.
Д/З: изучить стр. 85, записи в тетрадях, подготовить презентацию «Роль воды в жизни живых организмов»
Онлайн урок: Клеточная теория. Макро и микроэлементы клетки по предмету Биология ЕГЭ
Клеточная теория способствовала пониманию того, что клетка является самой мельчайшей единицей жизни, которой присущи все признаки живого (размножение, обмен веществ, дыхание и др.).
До изобретения микроскопа люди не знали о существовании клеток.
Прибор для изучения микромира,микроскоп. был изобретен приблизительно в 1590 году голландскими механиками Гансом и Захарием Янсенами.
На основе это этого микроскопа был создан сложный микроскоп Корнелиусом Дреббелем (1572–1634).
В 1665 году английский ученый-физик Роберт Гук (1635–1703) усовершенствовал микроскоп и технологию изготовления линз. Желая убедиться в улучшении качества изображения, он рассматривал под ним срезы пробкового дерева, древесного угля и срезы живых растений.
На срезах растений он обнаружил мельчайшие поры, которые были похожи на пчелиные соты, и назвал их клетками.
Во второй половине XVII века появились работы виднейших микроскопистов Марчелло Мальпиги (1628–1694) и Неемии Грю (1641–1712), также обнаруживших ячеистое (клеточное) строение многих растений.
Антони ван Левенгук самостоятельно разработал конструкцию микроскопа, принципиально отличавшуюся от уже существующей, и усовершенствовал технологию изготовления линз, которые достигали большего увеличения, что позволило открыть одноклеточных животных (инфузорий), а также бактерии и дрожжи.
В клетках растений обнаружил ядра, хлоропласты, утолщения клеточных стенок.
Описал и зарисовал почкование гидр.
Гуго фон Моль различил в клетках растений живое вещество и водянистую жидкость (клеточный сок), обнаружил поры.
Английский ботаник Роберт Броун (1773–1858) в 1831 году открыл ядро в клетках орхидей, затем оно было обнаружено во всех растительных клетках.
Матиас Шлейден (1804–1881) изучал развитие и дифференциацию разнообразных клеточных структур высших растений, рассмотрел в ядрах клеток чешуи лука округлые тельца-ядрышки (1842).
В 1827 году русский ученый-эмбриолог Карл Бэр обнаружил яйцеклетки человека и других млекопитающих и доказал формирование многоклеточного животного организма из единственной клетки- оплодотворенной яйцеклетки, а также сходство стадий зародышевого развития многоклеточных животных, которое наводило на мысль о единстве их происхождения.
Все научные открытия, которые были накоплены к середине XIX века, требовали обобщения, в результате и появилась клеточная теория.
В 1880 г. Уолтер Флемминг описал хромосомы и процессы, происходящие при митозе.
С 1903 г. стала развиваться генетика.
Начиная с 1930 г. стала бурно развиваться электронная микроскопия, что позволило ученым изучать тончайшее строение клеточных структур.
XX век стал веком расцвета биологии и таких наук, как цитология, генетика, эмбриология, биохимия, биофизика.
Без создания клеточной теории это развитие было бы невозможным.
Неожиданные колебания уровней микроэлементов в среде для культивирования клеток in vitro: caveat emptor
Андерсон Дж. Г., Эриксон К. М. (2011) Важность микроэлементов для неврологической функции. В: Preedy V, Watson R, Martin C (eds) Справочник по поведению, пище и питанию. Спрингер, Нью-Йорк, NY
Google ученый
Арредондо М., Уауи Р., Гонсалес М. (2000) Регулирование поглощения и транспорта меди в монослоях кишечных клеток при остром и хроническом воздействии меди. Biochem Biophys Acta 1474: 169–176
Biochem Biophys Acta 1474: 169–176
Статья PubMed CAS Google ученый
Баурели К.А., Келлехер С.Л., Лённердаль Б.О. (2004). Функциональные и молекулярные ответы сосущих крыс и кишечных клеток Caco-2 человека на обработку медью
Behrens I, Kissel T (2003) Влияют ли условия культивирования клеток на опосредованный носителем транспорт пептидов в монослоях клеток Caco-2. Eur J Pharmaceutical Sciences 19: 433–442
Статья CAS Google ученый
Fitzwalter B, Thorburn A (2015) Недавние исследования клеточной смерти и аутофагии.FEBS J 282 (22): 4279–4288
Статья PubMed PubMed Central CAS Google ученый
Gaetke LM, Chow-Johnson HS, Chow CK (2014) Медь: токсикологическая значимость и механизмы. Arch Toxicol 88: 1929–1938
Статья PubMed PubMed Central CAS Google ученый
Ламарк Т. и Йохансен Т. (2012) Агрефагия: избирательное удаление белковых агрегатов с помощью макроаутофагии.Международный журнал клеточной биологии, том 2012 г. Идентификатор статьи 736905
и Йохансен Т. (2012) Агрефагия: избирательное удаление белковых агрегатов с помощью макроаутофагии.Международный журнал клеточной биологии, том 2012 г. Идентификатор статьи 736905
Натоли М., Леони Б.Д., Д’Аньяно И., Зукко Ф., Фелсани А. (2012) Надлежащие методы культивирования клеток Caco-2. Toxicol in vitro 26 (8): 1243–1246
Статья PubMed CAS Google ученый
Ruemmele FM, Schwartz S, Seidman EG, Dionne S, Levy E, Lentze MJ (2003) Бутират-индуцированный апоптоз клеток Caco-2 опосредуется митохондриальным путем.Gut 52 (1): 94–100
Артикул PubMed PubMed Central CAS Google ученый
Сахни С., Бэ Д.Х., Янссон П.Дж., Ричардсон Д.Р. (2017) Механистическая роль химически различных ионов металлов в индукции аутофагии. Pharmacol Res 117: 118–127
Статья CAS Google ученый
Сантос С. , Сильва А.М., Матос М., Монтейро С.М., Альваро А.Р. (2016) Медь-индуцированный апоптоз в клетках Caco-2 и Hep-G2: экспрессия каспаз 3, 8 и 9, AIF и p53.Comp Biochem Physiol C Toxicol Pharmacol 185–186: 138–146
, Сильва А.М., Матос М., Монтейро С.М., Альваро А.Р. (2016) Медь-индуцированный апоптоз в клетках Caco-2 и Hep-G2: экспрессия каспаз 3, 8 и 9, AIF и p53.Comp Biochem Physiol C Toxicol Pharmacol 185–186: 138–146
Статья PubMed CAS Google ученый
Townsend AT, Miller KA, McLean S, Aldous S (1998) Определение меди, цинка, кадмия и свинца в моче с помощью ICP-MS высокого разрешения. J Anal At Spectrom 13: 1213–1219
Статья CAS Google ученый
Власак Дж., Ионеску Р. (2011) Фрагментация моноклональных антител.mABs 3: 253–263
Статья PubMed PubMed Central Google ученый
Yuk IH, Russell S, Tang Y, Hsu WT, Mauger JB, Aulakh RP, Luo J, Gawlitzek M, Joly JC (2015) Влияние меди на ячейки CHO: требования к ячейкам и соображения качества продукции. Biotechnol Prog 31 (1): 226–238
Статья PubMed CAS PubMed Central Google ученый
СЛЕДОВЫЕ И НЕСЛЕДОВЫЕ ЭЛЕМЕНТЫ В КЛЕТКАХ БУТЛЕНЗНЫХ ДЕЛЬФИНОВ (TURSIOPS TRUNCATUS): ВАРИАЦИИ В ЗНАЧЕНИЯХ ОТ ПОКАЗАТЕЛЕЙ ФУНКЦИИ ПЕЧЕНИ
Нарушения гомеостаза следовых и не следовых элементов были связаны как с нормальными физиологическими, так и с патологическими процессами у многих видов. Например, изменения в меди и цинке связаны с заболеваниями печени у людей и собак. Хотя заболевание печени было зарегистрировано у морских млекопитающих, связь заболевания печени с микроэлементами и не-следовыми элементами не установлена. Целью этого исследования было оценить потенциальные элементарные ассоциации с клинически значимыми изменениями ферментов печени афалин ( Tursiops truncatus ) и сравнить наблюдаемые ассоциации с тем, что было зарегистрировано у других видов.Образцы клеток крови были собраны у 37 здоровых дельфинов-афалин, поддерживаемых Программой морских млекопитающих ВМС (MMP), в период с 1991 по 1992 год. Двадцать один микроэлемент и не-следовые элементы были оценены вместе со стандартным профилем функции ферментов печени и микроэлементами. были определены ассоциации со специфическими ферментами печени. В этом исследовании из 21 оцененного элемента клеток крови 19 были измерены в пределах обнаруживаемых пределов по крайней мере в одном из образцов крови, и было обнаружено, что 10 микроэлементов связаны по крайней мере с одним из показателей функции печени.
Например, изменения в меди и цинке связаны с заболеваниями печени у людей и собак. Хотя заболевание печени было зарегистрировано у морских млекопитающих, связь заболевания печени с микроэлементами и не-следовыми элементами не установлена. Целью этого исследования было оценить потенциальные элементарные ассоциации с клинически значимыми изменениями ферментов печени афалин ( Tursiops truncatus ) и сравнить наблюдаемые ассоциации с тем, что было зарегистрировано у других видов.Образцы клеток крови были собраны у 37 здоровых дельфинов-афалин, поддерживаемых Программой морских млекопитающих ВМС (MMP), в период с 1991 по 1992 год. Двадцать один микроэлемент и не-следовые элементы были оценены вместе со стандартным профилем функции ферментов печени и микроэлементами. были определены ассоциации со специфическими ферментами печени. В этом исследовании из 21 оцененного элемента клеток крови 19 были измерены в пределах обнаруживаемых пределов по крайней мере в одном из образцов крови, и было обнаружено, что 10 микроэлементов связаны по крайней мере с одним из показателей функции печени. Многие из этих ассоциаций были задокументированы при различных формах заболеваний печени у других видов, включая ассоциации увеличения содержания меди и уменьшения содержания цинка как с повышенным уровнем аланинаминотрансферазы (ALT), так и с гамма-глутамилтрансферазой (GGT). Наблюдаемые аналогичные ассоциации между изменениями в крови и показателями функции печени афалин и других видов могут указывать на аналогичные патологические процессы и функции некоторых элементов. Учитывая результаты этого исследования, необходимы дополнительные исследования для дальнейшего выяснения связи следовых и не-следовых элементов с заболеваниями печени у афалин.
Многие из этих ассоциаций были задокументированы при различных формах заболеваний печени у других видов, включая ассоциации увеличения содержания меди и уменьшения содержания цинка как с повышенным уровнем аланинаминотрансферазы (ALT), так и с гамма-глутамилтрансферазой (GGT). Наблюдаемые аналогичные ассоциации между изменениями в крови и показателями функции печени афалин и других видов могут указывать на аналогичные патологические процессы и функции некоторых элементов. Учитывая результаты этого исследования, необходимы дополнительные исследования для дальнейшего выяснения связи следовых и не-следовых элементов с заболеваниями печени у афалин.
Кашив публикует исследование по визуализации микроэлементов в органеллах // Новости // Научный колледж // University of Notre Dame
Йоав Кашив, приглашенный научный сотрудник отдела физики, является ведущим автором недавно опубликованной статьи о прорывном успехе в визуализации микроэлементов в отдельных органеллах внутри клетки. Статья «Визуализация распределения микроэлементов в отдельных органеллах и субклеточных особенностях» была опубликована в феврале в журнале Scientific Reports.Сотрудниками Кашива являются Джотам Р. Остин II (Чикагский университет), Барри Лай, Волкер Роуз, Стефан Фогт (Аргоннская национальная лаборатория) и Малек Эль-Муайед (Северо-Западный университет).
Статья «Визуализация распределения микроэлементов в отдельных органеллах и субклеточных особенностях» была опубликована в феврале в журнале Scientific Reports.Сотрудниками Кашива являются Джотам Р. Остин II (Чикагский университет), Барри Лай, Волкер Роуз, Стефан Фогт (Аргоннская национальная лаборатория) и Малек Эль-Муайед (Северо-Западный университет).
Еще несколько лет назад исследователи изучали клетку как единое целое с точки зрения ее химического состава. Субъединицы клетки, называемые органеллами, такие как ядро или митохондрии, обычно изучаются в больших группах многих органелл определенного типа из многих клеток. В этом исследовании исследователи сосредоточились на отдельных органеллах, чтобы определить распределение таких элементов, как хлор, калий, кальций, кобальт, никель, медь, цинк и кадмий.Этот метод позволит исследователям сравнить состав отдельных органелл, например, из клеток здоровых и больных органов.
Измерение сочетает в себе просвечивающую электронную микроскопию (ТЕМ) и синхротронную рентгеновскую флуоресценцию (SXRF) с использованием двух линий луча в Advanced Photos Source (APS), синхротроне в Аргоннской национальной лаборатории. Один из этих лучей, Центр наноразмерных материалов (CNM), фокусирует рентгеновский луч до 40 нанометров, что в настоящее время является самым высоким разрешением рентгеновского излучения среди всех синхротронов в мире.Поскольку органеллы очень маленькие, высокое разрешение было решающим для успешных измерений. Тщательная подготовка образцов клеток также имела решающее значение для успеха.
Один из этих лучей, Центр наноразмерных материалов (CNM), фокусирует рентгеновский луч до 40 нанометров, что в настоящее время является самым высоким разрешением рентгеновского излучения среди всех синхротронов в мире.Поскольку органеллы очень маленькие, высокое разрешение было решающим для успешных измерений. Тщательная подготовка образцов клеток также имела решающее значение для успеха.
Проект начался, когда Кашив объединил усилия с Эль-Муайедом, эндокринологом, который стремился определить влияние кадмия на выработку инсулина и его связь с диабетом 2 типа. В конце концов, успех стал результатом того, что каждый сотрудник поделился своим опытом. «Мы не рассматриваем клетку как единое целое, мы фактически разбиваем ее на различные компоненты и смотрим, как химические элементы распределяются внутри клетки», – сказал Кашив.«Это открывает новые возможности для изучения отдельных компонентов клетки и их влияния на функцию клетки».
Контроль примесей в средах для клеточных культур
С момента своего первоначального развития еще в 1950-х годах разработка сред для культивирования клеток была затруднена из-за примесей, часто присутствующих в небольших количествах, трудно поддающихся описанию и прослеживаемых до их происхождения. Обычно в питательные среды требуется добавление сыворотки животных, которая выполняет функцию питания, но также может абсорбировать и связывать следовые примеси, которые могут препятствовать росту клеток.
Обычно в питательные среды требуется добавление сыворотки животных, которая выполняет функцию питания, но также может абсорбировать и связывать следовые примеси, которые могут препятствовать росту клеток.
Тем не менее, с более высокой чистотой реагентов и лучшей характеристикой стало возможным создать широкий спектр различных бессывороточных сред, имеющих особую ценность, когда белки, синтезированные сконструированными клетками, необходимо очистить от их резидентных сред. Это означает, что еще более важно отслеживать незначительные примеси в питательных средах.
GEN недавно опросил нескольких экспертов по вопросам, связанным с решением этих проблем. В составе панели:
Трисса Боргшульте, доктор философии , старший директор и руководитель отдела исследований и разработок в области биопереработки, MilliporeSigma
Винс Нгуен , старший инженер по разработке процессов, Precision Biosciences
Atherly Pennybaker , специалист по применению продуктов, InVitria
GEN : Из-за своей сложности примеси в средах для культивирования клеток может быть трудно обнаружить и измерить.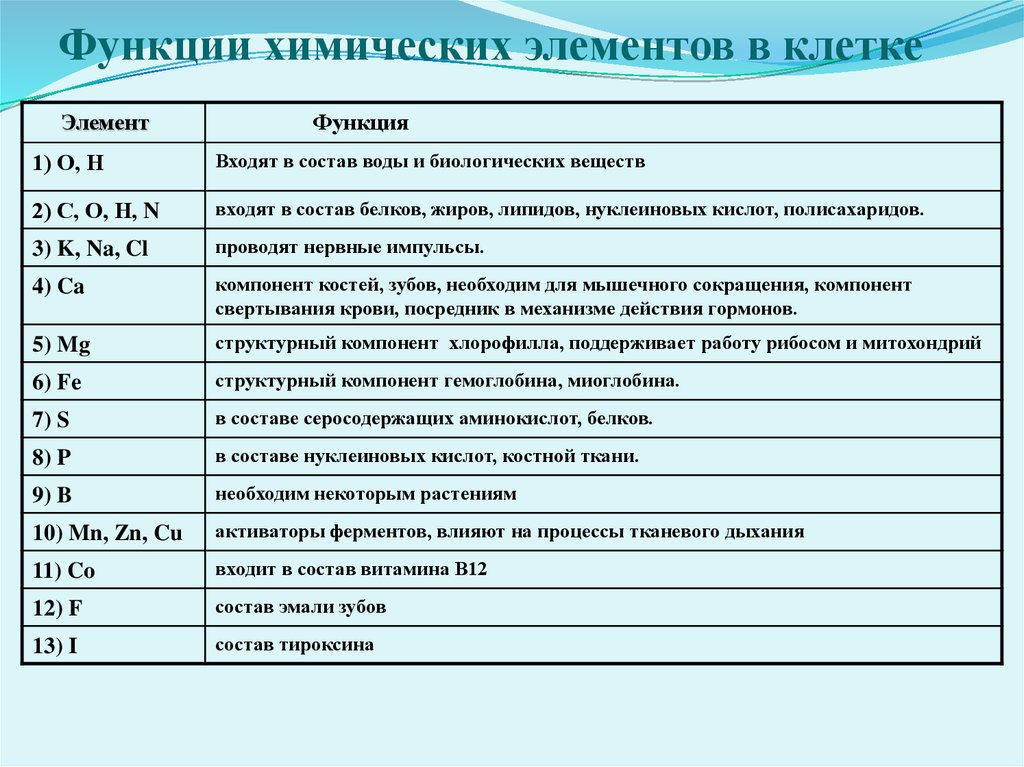 Следы металлов часто могут служить загрязняющими веществами и могут оказывать значительное влияние на качество и количество продуцируемого белка. Это проблема для вас при мониторинге ваших СМИ? И если да, то как вы за этим следите?
Следы металлов часто могут служить загрязняющими веществами и могут оказывать значительное влияние на качество и количество продуцируемого белка. Это проблема для вас при мониторинге ваших СМИ? И если да, то как вы за этим следите?
Borgschulte: В состав сред для культивирования клеток входит множество исходных материалов. Хотя цепочка поставок этого сырья остается относительно неизменной за последние 40 лет, то, как мы рассматриваем цепочку поставок и возможность вариабельности биопроцессов, изменилось.
Роль микроэлементов и их влияние на качество белков и продуктов хорошо задокументированы. Таким образом, введение микроэлементов путем добавления препарата имеет решающее значение. Вариации в этих критических компонентах были связаны с непреднамеренными примесями в преобладающих цепочках поставок сырья для культур клеток. Первый шаг в понимании и управлении изменчивостью – получение надежных данных об этих критически важных микроэлементах.
MilliporeSigma стремится предоставлять ученым и инженерам лучшие в своем классе лабораторные материалы, технологии и услуги, поэтому мы изучаем влияние микроэлементов.Теперь мы предлагаем тестирование готовой продукции на наличие микроэлементов, а также мониторинг нашей продукции и сырья с высоким риском в наших цепочках поставок.
Винс НгуенНгуен : С точки зрения качества проблема следов металлов связана с реакцией Фентона, в которой металл является катализатором, приводящим к образованию свободных радикалов. Этому противодействует тот факт, что пока клетки живы, среда для культивирования клеток является восстанавливающей средой.В результате в большинстве случаев следы металлов не являются проблемой. Конечно, никогда не бывает «одного размера для всех». Некоторые процессы чувствительны или просто ненадежны, и клетки могут потерять баланс между окислительным и восстановленным состояниями в присутствии избытка следов металла.
Конечно, существует множество потенциальных источников следов металлов, в том числе различия в расходных материалах от партии к партии. Когда есть отклонения в профилях IEX для процесса, источник расходных материалов – одно из первых мест, куда я бы посмотрел.
И наоборот, низкие уровни некоторых следов металлов также могут быть проблемой. Есть публикации, описывающие ситуации, когда низкий уровень меди может вызвать выработку лактата. В этом случае автор решил эту проблему, фактически добавив следы меди, чтобы перевести окружающую среду в немного более окислительное состояние.
Взгляды, выраженные на этом форуме, являются мнением респондента и не отражают политику или убеждения компании, в которой он работает.
GEN : Следы металлов также жизненно важны для оптимального роста и производительности. Какие подходы вы используете для регулирования уровней микроэлементов, включая медь, марганец, цинк и селен?
Atherly PennybakerBorgschulte: Источником микроэлементов для клеточных культур являются два основных источника: предполагаемые следовые количества металлов при добавлении в состав и непреднамеренные примеси следов металлов из сырья в преобладающей цепочке поставок клеточных культур.Для предполагаемых следов металлов мы разработали контролируемые процессы добавления микроэлементов на уровне частей на миллиард в среды для культивирования клеток. Что касается непреднамеренных металлических примесей, мы разработали программы мониторинга для сырья с высоким уровнем риска, чтобы включить такие ключевые источники, как соли железа, поскольку изменения в существующих цепочках поставок не всегда возможны.
GEN : Загрязнения в питательных средах могут возникать из различных источников, включая воду, добавленную сыворотку и различные химические компоненты.Каков ваш опыт в отношении наиболее частых источников загрязненных компонентов?
Borgschulte: MilliporeSigma всегда ориентировалась на потребности отрасли и решает те же самые сложные задачи. Что касается сред для культивирования клеток, то существенных изменений в преобладающих цепочках поставок не произошло. Любые наблюдаемые примеси присутствовали всегда. Переход к химически определенным рецептурам и усложнение методов измерения показателей качества белка выявили изменчивость цепочки поставок, поскольку не существует установленных правил для примесей, таких как микроэлементы.То, что приемлемо в качестве микроэлемента для одной компании и его протеин, может быть вредным для другой компании и ее протеина.
Лучшим проактивным инструментом является измерение примесей, а затем совместная работа с заказчиком для разработки стратегии управления изменчивостью, учитывая, что изменения в преобладающей цепочке поставок могут быть невозможны. Управление молекулами должно включать пределы толерантности к присущей изменчивости биопроцесса.
Pennybaker: Загрязнение – не новая проблема в этой отрасли.Чаще всего это происходит из-за вариабельности фетальной бычьей сыворотки (FBS) или сыворотки крови человека, что повышает риск попадания случайных инфекционных примесей в питательную среду. Хорошо известно, что существует несоответствие между партиями сыворотки и белков, полученных из сыворотки, но ее степень полностью не изучена. В некоторых случаях партии FBS могут демонстрировать более чем 10-кратную разницу в известных компонентах, помимо потенциального присутствия других неопределенных веществ.
Кроме того, руководящие принципы производства человеческого сывороточного альбумина требуют чистоты только 96%, что открывает дверь для неизвестных и потенциально биологически активных веществ и факторов, включая вирусные контаминанты.Были даже вспышки, связанные с более сложными продуктами на основе сыворотки, такими как фракция белков плазмы (PPF), которые указывают на дифференциальный профиль безопасности в этом классе компонентов, полученных из сыворотки. Для снижения рисков контаминации и высокой вариабельности добавление рекомбинантных белков сыворотки крови человека, которые не только демонстрируют более однородные пики RP-UPLC между партиями, но и устраняют необходимость в вирусспецифическом тестировании, представляет собой очень привлекательное решение.
GEN : Интересно, что вода действительно может быть чрезмерно очищена, и в этом случае она может быть реактивной и вызывать выщелачивание токсичных химикатов из технологических сосудов, используемых при приготовлении среды.Сталкивались ли вы когда-нибудь с этой необычной ситуацией и какие шаги вы предприняли, чтобы избежать ее или справиться с ней?
Borgschulte: Вода в чистом виде имеет ионную природу и может вступать в реакцию. MilliporeSigma следует тем же мировым стандартам использования промышленной воды, что и вода для инъекций для жидких препаратов и / или очищенная вода для стандартов ополаскивания сухой порошковой очисткой. Все жидкие составы созданы с буферными системами, которые, по нашему опыту, не представляли проблемы с точки зрения реакции с технологическими сосудами.Жидкие растворы имеют стандарты качества для pH и осмолярности, и изменение этих ключевых характеристик может указывать на проблему.
В равной степени все организации, занимающиеся биотехнологиями, включая MilliporeSigma, устанавливают внутренние стандарты для пассивации / повторной пассивации, выбирают чистящие средства высшего качества, которые могут снизить потребность в повторной пассивации, и устанавливают соответствующие стандарты для квалификации / повторной аттестации оборудования и процессы. В целом, эта тема не была областью, вызывающей озабоченность.
GEN : Эндотоксины, продукты грамотрицательных бактерий, также часто возникают при приготовлении и мониторинге питательных сред. Можете ли вы обсудить свой опыт с эндотоксинами: обнаружение, лечение, устранение неполадок?
Borgschulte: Мониторинг эндотоксинов и управление ими являются ключом к производству качественных культур клеток. Наша компания следует тем же глобальным компендиальным тестам для измерения эндотоксинов и устанавливает соответствующие методы мониторинга и контроля входящего сырья с высоким уровнем риска, ключевых этапов процесса и исходящей готовой продукции.
Pennybaker: Это отличный пример преимущества тестирования отдельных компонентов клеточной культуры на эндотоксин, чтобы контролировать их уровень в полной среде для культивирования клеток. Для наших конечных рекомбинантных белковых продуктов мы используем анализ кинетического хромогенного эндотоксина с лизатом амебоцитов limulus (LAL). Мы обнаружили, что этот метод лучше всех по своей способности не только определять наличие эндотоксинов, но и определять их количество. Этот уровень количественных данных значительно помогает в контроле качества и качества, а также может быть полезен для устранения неполадок, когда в культуральных средах возникают проблемы с эндотоксинами, которые можно проследить до одного компонента.
С производственной точки зрения наличие такого уровня контроля при составлении полностью химически определенной среды приводит к получению конечного продукта среды для культивирования клеток непревзойденного качества для конечного пользователя.
GEN : Свободные радикалы могут образовываться в определенных типах сред, подверженных воздействию флуоресцентного света. Как вы справляетесь с этой проблемой?
Pennybaker: Самым важным моментом в проблеме образования свободных радикалов является то, что профилактика является ключевым моментом.Простые шаги, такие как размещение напоминаний в лаборатории или непосредственно на бутылях с носителями, чтобы они не попадали в свет, и аликвоты меньших рабочих объемов, могут иметь большое значение для успешного снижения количества света. Бессывороточные среды в этом отношении еще более хрупкие, поэтому для оператора становится критически важным следовать надлежащим методам культивирования клеток для решения этой проблемы. Несмотря на важность проактивных шагов, окислительный стресс и образование свободных радикалов представляют собой неминуемую угрозу для технологии культивирования клеток.Эти свободные радикалы могут препятствовать клеточной антиоксидантной защите, поэтому крайне важно дополнять среду другими источниками антиоксидантов, которые могут поддерживать эти функции. Для этой цели часто используются обычные поглотители кислорода, такие как аскорбиновая кислота (витамин С), глутатион, мочевая кислота или даже альбумин.
Среда с химическим определением становится отличным инструментом в этом случае, потому что точно известно, какие компоненты способствуют предотвращению повреждения свободными радикалами и как они влияют на общую производительность культуры.
Borgschulte: При необходимости мы маркируем готовую продукцию и материалы в процессе производства надписью «Защищать от света» и отмечаем установленные процессы и процедуры для поддержки требований.
| Железо и медь | Farkas RH, et al., 2014 [21] | Сравнение глаукомных и контрольных сетчаток обезьян продемонстрировало повышенную экспрессию мРНК регулирующих железо белки.Повышенные уровни белков, регулирующих железо, при глаукоме полезны из-за их способности ограничивать окисление, связанное с железом. |
| Gye H.J. et al., 2016 [22] | Сывороточный ферритин стал предпочтительным маркером для оценки окислительного стресса, связанного с железом. Высокие уровни ферритина в сыворотке были независимо связаны с повышенным риском глаукомы. | |
| Hara H. et al., 1999 [23] | Ломеризин увеличивал церебральный кровоток на животных моделях без значительных побочных эффектов.Это говорит о том, что этот препарат может быть клинически полезным при состояниях, связанных с нарушениями кровообращения (таких как мигрень, глаукома нормального давления, головокружение и инсульт). | |
| Кальций | Al-Dabbagh N. et al., 2017 [24] | Мутация гена модульного кальций-связывающего белка 2 (SMOC2), связанного с SPARC, может быть фактором риска глаукомы, вероятно, вторичным по отношению к модификации биологической функции белков рецептора Са в тканях глаза. |
| Хартикайнен Х.et al., 2005 [25] | Кальпаин, широко распространенная кальций-чувствительная протеаза, играет роль в нейродегенеративных заболеваниях, таких как церебральная ишемия, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, множественный склероз и другие | |
| Головка КА et al., 2001 [26] | Измененный гомеостаз кальция делает нейроны более уязвимыми к окислительному стрессу | |
| Hohberger B. et al., 2018 [20] | Было обнаружено, что ингибиторы кальциевых каналов плазматической мембраны останавливают острую дегенерацию аксонов и улучшить регенерацию после повреждения зрительного нерва | |
| Houde M.et al., 2016 [27] | Исследования in vivo показали нейрозащитный эффект блокаторов кальциевых каналов. Более того, бета-адренорецепторы проявляют активность по блокированию кальциевых каналов, что может быть ответственным за нейрозащитные эффекты. | |
| Hurst S. et al., 2017 [28] | Животные, получавшие местно блокаторы кальциевых каналов, показали значительное снижение внутриглазного давления при стероид-индуцированной глаукоме. | |
| Iqbal Z. et al., 2002 [29] | Лечение антагонистом кальциевых каналов (нимодипин) значительно улучшило поле зрения и цветовое зрение у пациентов с глаукомой. | |
| Ishikawa K. et al., 2005 [30] | Пероральный нилвадипин увеличивал кровоток в дистальных ретробульбарных артериях при глаукоме нормального давления. | |
| Hara et al., 1999, 2004 [23,31] | Блокатор Са2 + каналов ломеризин увеличивает кровообращение в глазах и защищает нейрональные клетки в моделях на животных. Он может быть полезен в качестве терапевтического препарата против заболеваний сетчатки, которые включают нарушение глазного кровообращения (таких как глаукома и окклюзионные заболевания сосудов сетчатки). | |
| Kitazawa Y. et al., 1989 [32] | Пациенты с глаукомой низкого давления, получавшие антагонист Ca2 + нифедипин в течение 6 месяцев. У шести пациентов наблюдалось постоянное улучшение поля зрения. | |
| Селен | Phelps Brown N.A. et al., 1998 [33] | Чрезмерное употребление селена может увеличить заболеваемость глаукомой |
| Prasad A.S. et al., 2014 [34] | Высокая концентрация селена в плазме и средняя концентрация селена в водянистой влаге в значительной степени связаны с глаукомой. | |
| Prasanna G. et al., 2002 [35] | Средние уровни селена в водянистой влаге и в сыворотке крови пациентов с синдромом PEX были ниже, чем в контрольной группе. Эти результаты могут подтвердить роль нарушения системы антиоксидантной защиты в патогенезе синдрома PEX. | |
| Куигли Х.А. et al., 2006 [3] | Добавление селена (200 мг / день) было связано с развитием глаукомы. Риск был даже выше у тех, кто продолжал принимать селен после испытания. | |
| Цинк | DeToma A.S. et al., 2014 [36] | Сетчатка мышей в преглаукомном состоянии имели более высокие концентрации Mg, Ca и Zn, чем у мышей с глаукомой, и более высокие концентрации Mg и Ca, чем контрольные |
| Grahn B.H. et al., 2001 [37] | Добавка цинка кажется полезной для пациентов с диабетом. Zn как антиоксидант ослабляет действие ROS, поэтому он может защищать сетчатку от повреждения ROS, тем самым защищая от DR | |
| Newsome D.A. et al., 1995 [38] | Концентрация цинка снижается в глазах человека с признаками возрастной дегенерации желтого пятна (AMD), что свидетельствует о том, что дефицит цинка может привести к окислительному стрессу и повреждению сетчатки | |
| Noske W . et al., 1997 [39] | Цинк необходим для функционирования глаз. В сетчатке и пигментном эпителии сетчатки цинк взаимодействует с таурином и витамином А и модифицирует плазматические мембраны фоторецепторов, регулирует реакцию свет-родопсин, модулирует синаптическую передачу и служит антиоксидантом. | |
| Осборн Н.Н. et al., 2016 [40] | Цинк может быть вовлечен в светоиндуцированное повреждение сетчатки; однако механизмы светового повреждения сетчатки при патологии глаукомы остаются неизвестными. | |
| Магний | Ekici F. et al., 2014 [13] | Mg может защищать ганглиозные клетки сетчатки от окислительного повреждения за счет комбинированного воздействия на потенциал-зависимые кальциевые каналы, синтез глутатиона, перекисное окисление липидов и поддержание регуляции многие метаболические ферментативные реакции |
| Кумар А.R. et al., 2002 [41] | Mg важен для поддержания структурной и функциональной целостности нескольких жизненно важных тканей глаза | |
| Laganovska G. et al., 2003 [42] | Было показано, что дефицит Mg способствует вызывают дефектный механизм транспорта нейротрансмиттеров, митохондриальную дисфункцию, дефектную функцию тела Гольджи и дисфункцию процессинга белков, дегенерацию нейронов и апоптоз | |
| Lee SH et al., 2016 [43] | Mg играет решающую роль в транспорте Na + и K + в клетках.Это важный кофактор Na + / K + -АТФаза | |
| Lenartowicz M. et al., 2015 [44] | Mg увеличивает кровоснабжение зрительного нерва за счет расширения зрительных кровеносных сосудов | |
| Li X. et al., 2011 [45] | Введение Mg два раза в день в течение 1 месяца оказало положительное влияние на поле зрения | |
| Lillico A. et al., 2002 [46] | Лечение 300 мг цитрата магния в течение 1 месяца не изменили глазной кровоток, но вызвали некоторое улучшение поля зрения | |
| Молибден | DeToma A.S. et al., 2014 [36] | Повышенные и пониженные концентрации молибдена влияют на болезнь |
| Ионы натрия / катионы калия | Jünemann A.G.M. et al., 2018 [47] | Исследования изолированного зрительного нерва показали, что натрий снижает приток натрия и потенциально может быть эффективными нейропротекторами |
| Hains B.C. et al., 2005 [48] | Фенитоин (блокатор натриевых каналов) привел к нейрозащите RGC и аксонов зрительного нерва в экспериментальной модели глаукомы на животных | |
| Ramdas W.D. et al., 2018 [49] | Ранние исследования показали различия в концентрации в плазме между здоровыми людьми и пациентами с глаукомой | |
| Ribas V.T. et al., 2015 [50] | Смерть RGC является основной причиной глазных невропатий. Калиевые (K + ) каналы играют ключевую роль в модуляции электрических свойств клеток RG | |
| Roy Chowdhury U. et al., 2015 [51] | Присутствие совместной транспортной активности Na / K / Cl в клетки трабекулярной сети (TM) способны проверить гипотезу о том, что модуляция совместного транспорта Na / K изменяет внутриклеточный объем и, следовательно, проницаемость мембран TM-клеток. | |
| Roy Chowdhury U. et al., 2016 [52] | Блокада натриевого канала фенитоином приведет к нейрозащите RGC | |
| Roy Chowdhury U. et al., 2017 [53] | Доставляется перорально эффективен в защите нейронов, NS-7 (4- (4-фторфенил) -2-метил-6- (5-пиперидинопентилокси) пиримидин гидрохлорид новый Na + / Ca 2+ блокатор каналов , может защитить крысу сетчатка | |
| Рой Чоудхури У.et al., 2019 [54] | Роль внутриклеточной перегрузки Na + в ишемическом повреждении остро изолированных зрительных нервов крыс путем оценки электрических потенциалов (CAP) от зрительных нервов | |
| Saito S. et al., 2005 [55] | Кромакалим является гипотензивным агентом, действующим посредством активации Kir6.2, содержащих каналы K ATP , и его действие является аддитивным в сочетании с обычно используемым лекарством от глаукомы латанопростом | |
| Сакамото К.et al., 2004 [56] | Производные канала K ATP были оценены для контроля способности глаза снижать внутриглазное давление | |
| Salvatore S. et al., 2010 [57] | Новый класс терапевтических средств против глаукомы , открывая каналы K ATP , может влиять на трабекулярную сеть и регулирование внутриглазного давления. | |
| Sample PA et al., 1986 [58] | K ATP открыватели каналов – диазоксид и никорандилл – снижают внутриглазное давление путем специфической активации пути Erk1 / 2 в клетках глаза | |
| Savigni D.L. et al., 2013 [59] | Применение дигоксина, селективного ингибитора Na + / K + -АТФазы, для изоформы α2β3 фермента, эффективно снижает фармакологически индуцированное и базальное внутриглазное давление у кроликов. | |
| Schwalfenberg GK et al., 2017 [60] | АТФ-зависимые калиевые каналы (К АТФ каналы) в митохондриальных или плазматических мембранах могут обеспечивать защиту от ишемии сетчатки | |
| Sheck L., Davies J. et al., 2010 [61] | АТФ-зависимые калиевые каналы (К АТФ каналы) в митохондриальных или плазматических мембранах могут обеспечивать защиту от ишемии сетчатки | |
| Shoshani Y.Z. et al., 2012 [62] | В глиальных клетках Мюллера каналы K ATP регулируют ток сетчатки и играют ключевую роль в защите сетчатки от ишемических состояний, например, ишемического инсульта | |
| Siegner S.W. et al., 2000 [63] | каналы MaxiK и K ATP каналов были обнаружены в клетках трабекулярной сети глаза | |
| Silverstone B.et al., 1981 [64] | Открытие калиевых каналов может играть защитную роль за счет увеличения увеального оттока | |
| Silverstone B.Z. et al., 1990 [65] | KR-31378 ((2S, 3S, 4R) -N ” – циано-N (6-амино-3,4-дигидро-3-гидрокси-2-метил-2-диметоксиметил- 2Hбензопиран-4-ил) -N’-бензилгуанидин) в качестве сильнодействующего агента, открывающего каналы K ATP , на снижение внутриглазного давления и его защитное действие на RGC | |
| Скатчков С.Н. et al., 2002 [66] | Cromakalim показал снижение давления (на 30–40%) и возможности оттока (на 50–80%) | |
| Sourkes T.L. et al., 1972 [16] | Влияние обработки дексаметазоном на активность ко-транспорта Na / K / Cl и экспрессию белка-переносчика в клетках трабекулярной сети (TM) | |
| DeToma A.S. et al., 2014 [36] | Концентрация Mn была значительно увеличена у пациентов с синдромом псевдоэксфолиации (PEX) | |
| Марганец | Südhof T.C. et al., 2012 [18] | Уровень Mn отрицательно ассоциировался с диагнозом глаукома в популяционном исследовании 2680 человек в Южной Корее |
| Demirci F.Y. et al., 2006 [67] | Исследование связи между уровнями трех тяжелых металлов и возникновением открытоугольной глаукомы (OAG) с низким и высоким внутриглазным давлением | |
| Тяжелые металлы [ртуть (Hg) , свинец (Pb), кадмий (Cd), хром (Cr), никель (Ni), висмут (Bi), полуметаллы] | Südhof TC et al., 2012 [18] | Уровень тяжелых металлов в крови был отрицательно связан с диагнозом глаукома в популяционном исследовании с участием 2680 человек в Южной Корее |
| Tham Y.C. et al., 2014 [8] | Накопление Hm может быть нераспознанным фактором риска не зависимой от давления глаукомной оптической невропатии | |
| Tykocki N.R. et al., 2010 [68] | Известно, что свинец вызывает повреждение тканей в результате окислительного стресса, перекисного окисления липидов и повреждения ДНК |
Нарушение гомеостаза микроэлементов из-за анеуплоидии как объединяющей темы в этиологии рака
Рефераты
Рефераты для ученых Хотя десятилетия исследований рака твердо установили множество «отличительных черт рака» 1,2 , геномный ландшафт рака еще предстоит полностью понять.В частности, остается загадкой феномен анеуплоидии – увеличения или уменьшения крупных участков генома, то есть целых хромосом или хромосомных плеч – и того, почему большинство раковых клеток являются анеуплоидными. Еще одно частое наблюдение при многих различных типах рака – нарушение регуляции гомеостаза микроэлементов меди, цинка и железа. Концентрация меди заметно повышается в раковой ткани и плазме крови больных раком, тогда как уровни цинка обычно снижаются. 4–9 .Здесь мы обсуждаем гипотезу о том, что нарушение гомеостаза микроэлементов и феномен анеуплоидии могут быть связаны. Наш предварительный анализ геномных данных для различных типов опухолей, в основном из проекта Атлас генома рака (TCGA), предполагает, что прирост и потеря генов-переносчиков металлов происходят часто и хорошо коррелируют с уровнями экспрессии генов-переносчиков. Таким образом, они могут обеспечить преимущество избирательного роста, приводящего к развитию рака, на ранних и, возможно, более поздних стадиях развития рака.Эта идея согласуется с недавними наблюдениями на дрожжах, которые предполагают, что за счет увеличения и уменьшения хромосом клетки могут быстро адаптироваться к новым источникам углерода 10 , нехватке питательных веществ 11 , а также к токсичности меди 12 . При развитии рака у человека возможные управляющие события могут включать, среди прочего, усиление генов переносчиков цинка SLC39A1 и SLC39A4 в плечах хромосом 1q и 8q, соответственно, и потери генов переносчиков цинка SLC30A5 , SLC39A14 и SLC39A6 на 5q, 8p и 18q.Повторяющееся увеличение 3q может быть связано с геном транспортера железа TFRC , а потеря 13q – с геном транспортера меди ATP7B . Изменяя гомеостаз клеточных микроэлементов, такие события могут способствовать инициированию злокачественной трансформации. Интересно, что ослабление или сверхэкспрессия некоторых из этих генов-переносчиков металлов, как было показано, приводит к злокачественному поведению клеток in vitro. Последовательно было показано, что цинк влияет на ряд наблюдаемых характеристик «признаков рака», включая репарацию ДНК, воспаление и апоптоз, например.грамм. через его эффекты на передачу сигналов NF-каппа B. Мы называем эту модель гипотезой «рак переносчика металла анеуплоидии» (AMTC) и находим ее совместимой с канцерогенной ролью точечных мутаций и изменений числа фокальных копий в установленных генах-супрессорах опухолей и онкогенах (например, MYC , MYCN , TP53 , PIK3CA , BRCA1 , ERBB2 ). Мы предлагаем ряд подходов к тому, как эту гипотезу можно проверить экспериментально, и кратко касаемся возможных последствий для этиологии рака, метастазирования, лекарственной устойчивости и терапии.
Абстракция для детей Мы, люди, состоят из множества очень маленьких строительных блоков, которые называются клетками. Эти клетки можно увидеть в микроскоп, и они знают, как расти и что делать, исходя из информации о ДНК их хромосом. Иногда, если эта информация искажена, клетка может сойти с ума и начать бесконтрольно расти, даже в тех местах тела, где этого не должно быть. Этот процесс называется раком – ужасной болезнью, от которой люди очень болеют. Ученые не понимают, что именно заставляет клетки сходить с ума, поэтому было бы неплохо выяснить.Много лет назад ученые заметили, что хромосомы в этих раковых клетках отсутствуют или удвоены, но не смогли найти этому объяснения. Совсем недавно ученые обнаружили, что драгоценные металлы для нашего тела, которые не являются золотом и серебром, а цинком, железом и медью, не содержатся в нужных количествах в этих безумных раковых клетках. Кажется, что цинка и железа недостаточно, но слишком много меди, и, опять же, ученые не совсем понимают, почему. Итак, есть много вопросов без ответа об этих сумасшедших раковых клетках, и в этой статье мы описываем довольно простую идею о том, как числа хромосом и металлы могут быть связаны: мы думаем, что недостающие или удвоенные хромосомы производят меньше или больше переносчиков цинка, железа. и медь.В результате в раковых клетках остается мало цинка и слишком много меди, и эти изменения способствуют их неконтролируемому росту. Если бы эта идея была верной, многие люди были бы в восторге от нее. Но сначала эту идею нужно исследовать более глубоко в лаборатории, на компьютере и в больницах. Поэтому мы размещаем его в Интернете, чтобы другие люди тоже могли подумать и поработать над нашей идеей. Теперь есть множество способов проводить захватывающие эксперименты, и мы надеемся, что с их результатами мы сможем лучше понять, почему раковые клетки сходят с ума и как врачи могут улучшить свои методы лечения, чтобы помочь пациентам в будущем.
Реферат для взрослых Сто лет назад было высказано предположение, что рак – это заболевание хромосом, на основании наблюдений, что целые хромосомы или хромосомные ветви отсутствуют или дублируются в геномах клеток опухоли. Это явление называется «анеуплоидией» и наблюдается при большинстве видов рака, включая рак груди, легких, простаты, мозга и другие виды рака. Однако неясно, какие гены могут быть ответственны за это наблюдение или является ли это явление только побочным эффектом рака, не имеющим значения, поэтому важно выяснить.Второе наблюдение, полученное в результате фундаментальных исследований, заключается в том, что в опухолевых клетках изменяются концентрации нескольких питательных микроэлементов, особенно микроэлементов цинка, меди и железа. В этой статье мы предполагаем, что анеуплоидия является причиной этих изменений и что вместе эти два явления ответственны за некоторые из известных признаков или характеристик, которые известны от раковых клеток: быстрый рост, ускользание от разрушения иммунной системой и плохой рост. Ремонт ДНК. Идея новая и еще не опробована.Мы называем это гипотезой «рак переносчика металлов анеуплоидии» (AMTC). Чтобы проверить нашу идею, мы использовали обширную информацию, которая была предоставлена международными проектами, такими как Проект генома человека или Проект Атласа генома рака. Действительно, мы обнаружили, что многие гены-переносчики цинка, железа и меди в геноме подвержены анеуплоидии. В то время как здоровая клетка имеет две копии каждого гена, некоторые опухолевые клетки имеют только одну или три копии этих генов. Кроме того, количество белка и активность этих переносчиков металлов, по-видимому, коррелируют с этим числом копий гена, по крайней мере, мы видим, что промежуточные молекулы и предшественники белков, называемые матричной РНК, хорошо коррелируют.Таким образом, мы обнаружили, что общедоступные данные совместимы с нашей предполагаемой связью между переносчиками металлов и раком. Кроме того, мы выявили сотни исследований по биологии цинка, эволюционной биологии, геному и раку, которые также кажутся совместимыми. Например, риск рака увеличивается у пожилых людей, а также у людей с ожирением, он также увеличивается после определенных бактериальных или вирусных инфекций и из-за употребления алкоголя. В соответствии с гипотезой AMTC и, в частности, с идеей о том, что внешние изменения концентрации цинка в органе или ткани могут запускать самые ранние стадии развития опухоли, все эти факторы риска коррелировали с изменениями цинка или других микроэлементов.Однако, поскольку дополнительные эксперименты для проверки гипотезы AMTC еще не проводились, прямые доказательства нашей гипотезы все еще отсутствуют. Однако мы надеемся, что наша идея будет способствовать дальнейшим исследованиям с целью лучшего понимания рака – в качестве первого шага к его профилактике и разработке улучшенных противораковых методов лечения в будущем.
Микроэлементы
Оценка пробирок VACUETTE® Trace Elements для определения микроэлементов
Белые статьи /
PDF, 148 КБ
Poster_Venous Blood Collection
Плакат – Информация /
PDF, 2 МБ
PSDS_VACUETTE® Пробирка для забора крови Пробка
Паспорт безопасности продукта /
PDF, 119 КБ
/ Документ, содержащий информацию о безопасности и гигиене труда
PSDS_VACUETTE® Винтовые крышки
Паспорт безопасности продукта /
PDF, 119 КБ
/ Документ, содержащий информацию о безопасности и гигиене труда
Система забора эвакуированной крови (США)
Инструкция по применению IFU /
PDF, 223 КБ
/ ТОЛЬКО ДЛЯ США!
PSDS_Trace Elements Микроэлементы VACUETTE® Z без добавок
Паспорт безопасности продукта /
PDF, 121 КБ
/ Документ, содержащий информацию о безопасности и гигиене труда
Методы взятия крови VACUETTE®
Брошюра /
PDF, 2 МБ
Руководство по преаналитике VACUETTE®
Брошюра /
PDF, 1 МБ